1������� ʵ�������������������������з�����ȡ�ģ�
4HCl��Ũ��+MnO2
Cl2��+MnCl2+2H2O
��1���÷�Ӧ�����ӷ���ʽΪ?��
��2�����ƿA��ʢװ���DZ���ʳ��ˮ��ע�������ڱ���ʳ��ˮ���ܽ�Ⱥ�С�����Ȼ����ڱ���ʳ��ˮ�е��ܽ����ܴ���������?��
��3����������ˮ�����ԣ��������ж������о��ҵĴ̼��ԣ�������������������ж���������������ֱ����������У�����Ⱦ������ʵ�����п���?��Һ�������ж�������β����
��4����Ũ����80mL������Һ�ܶ�Ϊ1.19g/cm3�����ʵ���������Ϊ36.5%����MnO2��ַ�Ӧ��������5.6L����״��������������Ũ��������ʵ���Ũ��Ϊ?����������HCl�����ʵ���Ϊ?��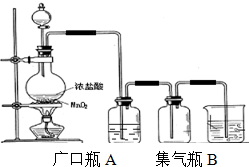
�ο��𰸣�
���������
�����Ѷȣ�һ��
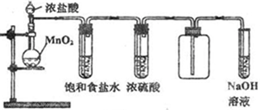
2������� ʵ�������ö������̸�Ũ���ᷴӦ�Ʊ����﴿�������������д�ʵ�飬����������ͼ��
��1������������������ȷ˳���ǣ�����ӿڴ�����ĸ����______��______��______��______��______��______��______��______��
��2����װ���У��ٱ���ʳ��ˮ���������______Ũ�������������______��
�ο��𰸣���1��ʵ��װ�õ�����˳��Ϊ������װ�á�����װ�á��ռ�װ�á�β������װ�ã���Ϊ�ռ��������壬���Գ���װ���г����ܽ������ε��ܳ�������Ϊ����ʳ��ˮ����ˮ��Ũ��������ˮ�ԣ����������ӱ���ʳ��ˮװ�ú�����Ũ����װ�ã��ռ�װ���У���Ϊ������Ũ�ȴ��ڿ����ģ����Գ����ܽ����̵��ܳ�����
�ʴ�Ϊ��E-C��D-A��B-H��G-F��
��2���Ȼ��⼫������ˮ������������ˮ������ˮ��Ӧ��Cl2+H2O=H++Cl-+HClO��ʳ��ˮ��Һ�е������������������ܽ⣬�����������ܽ�ȣ�Ũ��������ˮ�ԣ��Ҳ���������Ӧ�����Կ���Ũ�������������
�ʴ�Ϊ����ȥ�ӷ�����HCl���壬����C12��ˮ�е��ܽ⣻����ˮ����������Cl2��
���������
�����Ѷȣ���
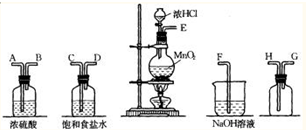
3������� ������ʾ�����������ڴ����а���ȼ�ա�ijУ��ѧС��ѧ���������װ�ã�ͼ�����еȼг�װ������ȥ�����а����������ڲ�ͬ�����·�Ӧ��ʵ�飮
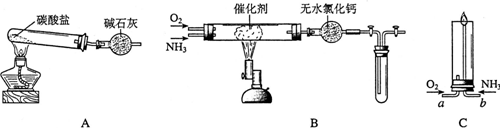
��1����װ��A��ȡ����������İ��������Թ���̼���εĻ�ѧʽ��?����ʯ�ҵ�������?��
��2���������İ��������������ͨ��װ��B������Ϊ��ʯ�ޣ��У��þƾ���Ƽ��ȣ�
�ٰ��������Ļ�ѧ����ʽ?���Թ��������Ϊ����ɫ���÷�Ӧ�Ļ�ѧ����ʽ��?��
��ֹͣ��Ӧ�������ر�B������������һ��ʱ����Թܽ����ˮ�У��Թ���������ɫ��dz�����ϻ�ѧ����ʽ˵��ԭ��?��
��3����������������A�����İ����ֱ��a��b���ܽ�����ͨ�˵�װ��C�У�����b���϶˵�ȼ������
��������ͨ����Ⱥ�˳����?����������?
�ڰ���ȼ�յĻ�ѧ����ʽ��?��
�ο��𰸣���1��̼���μ��ȷֽ��ܲ���NH3��ֻ�У�NH4��2CO3��NH4HCO3����ֽ�����Ļ������ͨ����ʯ�Һ�CO2��H2O�����գ��ɵõ�������NH3���ʴ�Ϊ����NH4��2CO3?��NH4HCO3��?����ˮ�Ͷ�����̼��
��2����NH3�����O2�ڴ��������������·�����Ӧ��4NH3+5O2����.��4NO+6H2O��ͨ����ˮCaCl2��δ��Ӧ���NH3�����ɵ�H2O�����գ����ɵ�NO���Թ��ڱ�������O2����Ϊ����ɫ��NO2���壬����ʽΪ��2NO+O2�T2NO2��
�ʴ�Ϊ��4NH3+5O2?����.��4NO+6H2O��2NO+O2�T2NO2��
�ڽ��Թܽ����ˮ�У�����2NO2��g��
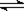
?N2O4��g����H��0������ӦΪ���ȷ�Ӧ�����¶Ƚ���ʱ��ƽ��������Ӧ�����ƶ������ֺ���ɫ��NO2ת��Ϊ��ɫN2O4������ɫ��dz���ʴ�Ϊ��2NO2?

?N2O4 ��H��0������ƽ��������Ӧ�����ƶ�����ɫ��dz��
��3������װ��C�϶˿��ڣ�Ҫ��ȼNH3������ͨ��O2����ͨ��NH3����Ϊ����ͨ��NH3��NH3�ڿ����в��ܵ�ȼ��NH3�ݳ��������Ⱦ��NH3�ڴ�����ȼ�յĻ�ѧ����ʽΪ��4NH3+3O2?��ȼ?.?2N2+6H2O��O2�û�N2����
�ʴ�Ϊ����ͨO2����ͨNH3������ͨNH3�������ڿ����в���ȼ�գ��ݳ���ɻ�����Ⱦ��4NH3+3O2??��ȼ?.?2N2+6H2O��
���������
�����Ѷȣ���
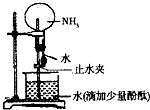
4��ѡ���� ��ͼ��ʵ���ҽ��а�����ˮ����Ȫʵ��װ�ã�������������ȷ���ǣ�������
A����ʵ��˵��������һ�ּ�������ˮ������
B��������ƿ�е�Һ����ɫ����ɫ��Ϊ��ɫ��˵����ˮ�м���
C���γ���Ȫ��ԭ���ǰ�������ˮ����ƿ�ڵ���ѹС�ڴ���ѹ
D�����������氱�������ô�װ��Ҳ�ɽ�����Ȫʵ��