1������� �ס��ҡ�����λͬѧ�ֱ������¼ס��ҡ�������ʵ��װ�ü���ѧҩƷ�����м�ʯ��Ϊ�����������ƺ���ʯ�ҵĻ�����ȡ�������������̽�������ش��������⣺
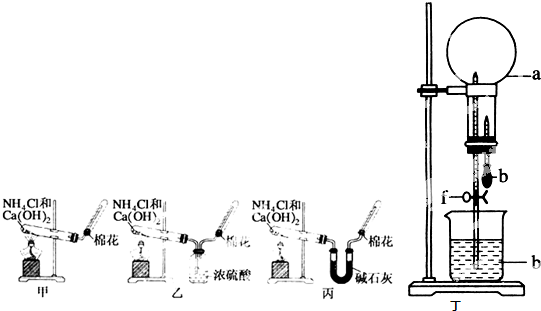
��1����λͬѧ��ȡ�����Ļ�ѧ����ʽΪ��______��
��2����λͬѧ���������ſ������ռ���������������ˮ������ԭ����______
A������������ˮ��������B��������������ˮ
C�������ܶȱȿ�����D�������ܶȱȿ���С
E�������ܶȱ�ˮ��F�������ܶȱ�ˮС
��3����λͬѧ������װ����ȡ����ʱ��������ͬѧû���ռ����������ռ�������������Ҫԭ����______���û�ѧ����ʽ��ʾ����
��4�����鰱���Ƿ��ռ����ķ�����______��
A���ŵ��а����ݳ�
B������������
C����ʪ��ĺ�ɫʯ����ֽ���Թܿڼ��飬������ֽ����
D����ʪ�����ɫʯ����ֽ���Թܿڼ��飬������ֽ���
��5����λͬѧ����Ϊ���ǵ�ʵ��װ��Ҳ�����ڼ���̼����粒�����ȡ�����İ��������ж��ܹ��ﵽʵ��Ŀ����______����ס������ҡ���������
��6��Ҫ�õ�����İ�����ѡ��______���������
A����ʯ�ң�CaO��NaOH�Ļ���
B��Ũ����
C��Ũ����
D������������Һ
��7������ͼ��װ�ý�����Ȫʵ�飬��ƿ����װ�����ﰱ������״����������ˮ������IJ�����______��
2������� ��ͼ��ʾ��û��ͨ������������Ʊ�����ʱ��Ƶ�װ�ã�ͼ��a��b�ǿɿ��Ƶĵ������У��������ڱ����Ȼ�����Һ�е��ܽ�Ƚ�С����
��1������A��������______��ˮ����Ӧʢ�ŵ���______���ձ���ʢ�ŵ���______����ƿ�з�Ӧ�Ļ�ѧ����ʽ______��
��2�����ռ�����ʱ��Ӧ______��������ο���a��b��
��3����Ҫ�Ƶñ�״���µ�Cl20.672L����������ҪMnO2��������______g��������������ʵ���______mol
��4����Ҫ����������ˮ��HClO��Ũ�ȿɼ���______
A��ʳ��B��ˮC��CaCO3D��NaOH��

3������� ����װ�����ڶ������̺�Ũ�����ڼ��������·�Ӧ��ȡ�����������������
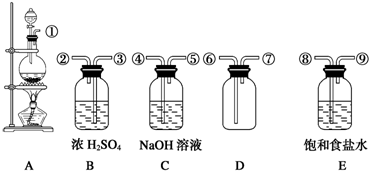
��1����װ��A��E�У��Т١�����ӿڣ��ñ�ű�ʾ�����ĵ���������˳������Ϊ______��
��2��Bƿ��ŨH2SO4��������______��Eƿʢ�еı���ʳ��ˮ��������______��
��3��Cƿ��ʢ��NaOH��Һ��Ϊ��______���䷴Ӧ�Ļ�ѧ����ʽ��______��
4��ʵ���� ������ˮ�Ȼ��������汸�á�������������ͼ��ʾ������Ũ���ᡢˮ�������ռ���ۡ��������̡�Ũ���ᡢ��ʯ�ң���Ҫ�ɷ�ΪCaO�� NaOH����ʳ�ι���Ȱ����Լ���
��Ƶ���ȡ�����ǣ������� �� ������������ �� ���Ȼ���
�����ϵ�֪����ˮAlCl3������ˮ���ö����ʣ�AlCl3������
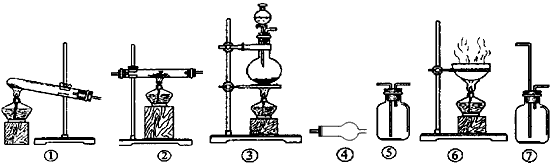
��ش��������⣺
��1��������������ѡȡ����ļ��֣����ӳ�һ������ˮ�Ȼ���������װ�ã���ǰ��˳����дͼ�ı�ţ������ظ�ʹ�ã����������______��______��______��______��______�� ��
��2��д��ʵ 91EXAm.org��������йط�Ӧ�Ļ�ѧ����ʽ(����2��)��
________________________��______________________________
��3����������װ����������Ӣܵ�������____________________________________
5������� ij�о���ѧϰС�������һϵ�л�ѧʵ����ָ�����طֽ��ĺ���Ԫ�صĻ����ﶼ�ܺ�Ũ���ᷴӦ�Ƶ��������̻�����Ļ�ԭ���ﶼ��MnCl2���磺K2MnO4+8HCl�TMnCl2+2Cl2��+2KCl+4H2O���������ֽ���������һЩ�йض�����ʵ�飬��Ҫ����ջ���㣨����������ۺϳɱ�״������
��1����ȡ��15.8g?KMnO4��ĩ�������Թ��м��ȳ�ַ�Ӧ���ռ�������������______����ȡ31.6g?KMnO4��ĩ���������ᷴӦ���ռ������������______��
��2����31.6g?KMnO4��ĩ����һ��ʱ�䣬�ռ���1.12L�����ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȣ����ռ������������______��
��3����a?mol?KMnO4��ĩ����һ��ʱ�䣬�ռ���V1L�����ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȷ�Ӧ��ֺ����ռ����������V2L����V2=______����a��V1�����