|
|
|
高中化学知识点总结《水的电离平衡》考点预测(2017年强化版)(一)
2017-11-05 22:17:00
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、填空题 常温下,将某一元酸HA和KOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表。请回答下列问题。

(1)从①实验结果分析,HA是_______酸(选填“强”或“弱”);该混合溶液中离子浓度由大到小的顺序是______________。
(2)②实验所得混合溶液中由水电离出的c(OH-)=_______mol・L-1。
(3)③实验中c1_______0.2 (选填“=”或“>”或“<”)。混合液中离子浓度c(A-)与c(K+)的大小关系是_______。
(4)④实验结果可知混合液中离子浓度c(A-)与c(K+)的大小关系是______________。
2、实验题 (10分)某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1 mol?L-1的盐酸和0.1mol?L-1的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol?L-1的氢氧化钠溶液滴定,需用去VmL达滴定终点;
④加入25.00mL0.1mol?L-1的盐酸溶液。
(1)写出实验过程中第一次滴定①-④的编号顺序______________。
(2)下图所示的仪器中配制0.1mol?L-1盐酸和0.1mol?L-1氢氧化钠溶液肯定不需要的仪器是(填序号)_________,配制上述溶液还需要的玻璃仪器是(填仪器名称)__________。
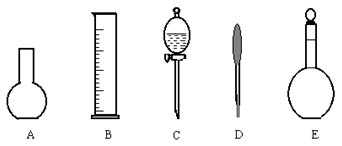
(3)配制上述溶液应选用的容量瓶的规格是(重复滴定一次)__________________。
A.50mL、50mL
B.100mL、100mL
C.100mL、150mL
D.250mL、250mL
| (4)写出有关的化学方程式_____________________ 。
3、选择题 25℃时pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得混合液的pH=11,则NaOH溶液与 H2SO4溶液的体积比是
A.1∶9
B.1∶11
C.9∶1
D.11∶1
|
4、选择题 下列说法正确的是:
A.相同温度时,1mol/L氨水与0.5mol/L氨水中,C(OH-)之比是2∶1
B.1mol/L NH4Cl溶液中 C(NH4+) = C(Cl-)
C.0.1mol/LCH3COONa溶液中加少量CH3COOH溶液,使溶液呈中性,此时混合液中C (Na+) =" C" (CH3COO-)
D.硫化钠溶液中,C (Na+) =" 2" C (S2-)
5、选择题 室温下,在pH=12的某溶液中,有甲、乙、丙、丁四位同学计算出由水电离出的c(OH-)的数据分别为甲:1.0×10-7mol・L-1;乙:1.0×10-6mol・L-1;丙:1.0×10-2mol・L-1;丁:1.0×10-12 mol・L-1。其中你认为正确的数据是
[? ]
A.甲
B.乙
C.丙
D.丁