1��ʵ���� 20����10�֣�ij�����ؾ�ʯ����Ч�ɷ���BaSO4��Ϊ��Ҫԭ����ȡBa(OH)2��8H2O�����ʾ��ͼ���£�

��֪��i��BaSO4(s)��2C(s)��2CO2(g)��BaS(s) ��H1��+226.2 kJ/mol
C(s)��CO2(g)��2CO(g) ��H2��+172.5kJ/mol
ii��ijЩ���ʵ��ܽ�ȣ�g/100g�����
| 10��
| 20��
| 40��
| 60��
| 80��
|
Ba(OH)2��8H2O
| 2.48
| 3.89
| 8.22
| 20.9
| 101
|
NaOH
| 98.0
| 109
| 129
| 174
| 314
|
NaCl
| 35.8
| 35.9
| 36.4
| 37.1
| 38.0
|
BaCl2
| 33.5
| 35.8
| 40.8
| 46.2
| 52.5
|
�ش��������⣺
��1��̿���ؾ�ʯֱ�ӷ�Ӧ���Ȼ�ѧ����ʽ�ǣ�BaSO4(s)��4C(s)��BaS(s)��4CO(g) ��H=____kJ/mol��
��2����BaCl2��Һ��ͨ����ͬ;���õ�Ba(OH)2��8H2O��
;��1��

�ٵõ�����1�����ӷ���ʽ��______��
�ڹ���2��ˮ��Ӧ�Ļ�ѧ����ʽ��______��
;��2��
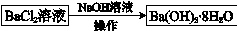
;��2�еġ��������Ǽ���Ũ������ȴ�ᾧ�����ˡ����������ܽ�ȼ������������ʱ������¶���______���ܴӻ��Һ�еõ�Ba(OH)2��8H2O�����ԭ����______��
��3��������Һ1�м���CuO��ĩ����ֱ�ӵõ���Ba(OH)2��8H2O�����CuS����Һ����Ӧ��ѧ����ʽ��______��������Һ���ȵ�80������Ũ�������ȹ��ˣ���ȴ��Һ�����£��ٹ��ˣ����ɵõ�Ba(OH)2��8H2O���塣���������г��ȹ��˵�ԭ����______��
2������� CH4?��һ����ࡢ��Ч�����������Ļ������ܵ�ȼ�ϣ���ȼ����Ϊ890.3KJ?mol-1����������Ϊȼ�ϵ�ص�ȼ�ϣ�
��1��д������ȼ�յ��Ȼ�ѧ����ʽ��______��
��2����֪H2��g����C��s����ȼ���ȷֱ���285.8KJ?mol-1��393.5KJ?mol-1����ӦC��s��+2H2��g��=CH4��g���ķ�Ӧ�ȡ�H=______��
��3���Լ��顢����������������ҺΪԭ�ϣ����Ե缫Ϊ�缫���Թ���ȼ�ϵ�أ��õ�صĸ�����ӦʽΪ��______��
��4���ã�3���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500ml���з�̪��NaCl��Һ��װ����ͼ��ʾ��
����д�������������������۲쵽������______��
�ڵ�ȼ�ϵ������2.8L?O2����״���£�ʱ�������ʱNaCl��Һ��pH=______��������Һ��������䣬����ȫ������Һ���ݳ�������Y��ͨ���ĵ��ӵ����ʵ���Ϊ��______��
�۵��֮��Ҫʹ��Һ�ָ�ԭ״��Ӧ������Һ�м�������______�������ƣ�����Һ��Cl-����______�����X����Y������
3��ѡ���� 2008�걱�����˻��������ֻ��̼��������Ԫ�صı�����ȼ�ϣ�ȼ�պ�ֻ����CO2��H2O���Ի�������Ⱦ����������ɫ���˵ľ�����֪1g�������ȼ������CO2�����Һ̬ˮ���ų�50.405kJ�������������Ȼ�ѧ����ʽ��ȷ���ǣ� ? ��
A��C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=-50.405kJ/mol
B��C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=+2217.82kJ/mol
C��C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=+50.405kJ/mol
D��C3H8��g��+5O2��g���T3CO2��g��+4H2O��l����H=-2217.82kJ/mol
4��ѡ���� ��֪��(1)Zn(s)��1/2O2(g) = ZnO(s)����H =��348.3 kJ/mol��(2)2Ag(s)��1/2O2(g) = Ag2O(s)����H =��31.0 kJ/mol����Zn(s)��Ag2O(s) = ZnO(s)��2Ag(s)��?��H���ڣ� ��
A����317.3 kJ/mol
B����379.3 kJ/mol
C����332.8 kJ/mol
D��317.3 kJ/mol