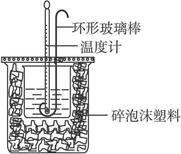
1��ʵ���� ʵ������50 mL 0.50 mol��L-1���ᡢ50 mL 0.55 mol��L-1 NaOH��Һ����ͼ��ʾװ�ý��вⶨ�к��ȵ�ʵ�飬�õ����е����ݣ�
ʵ�����
| ��ʼ�¶�t1/��
| ��ֹ�¶�t2/��
|
����
| NaOH��Һ
|
1
| 20.2
| 20.3
| 23.7
|
2
| 20.3
| 20. 5
| 23.8
|
3
| 21.5
| 21.6
| 24.9
|
������������⣺
(1)ʵ��ʱ�û��β�����������Һ�ķ�����_____________________________________��
������ͭ˿��������滷�β�������������__________________________________��
(2)�����ݴ�����t2-t1="3.4" �档���ʵ���õ��к��Ȧ�H=_________�������NaOH��Һ���ܶȰ�1 g��cm-3���㣬��Ӧ������Һ�ı�����(c)��4.18 J��(g����)-1���㡳��
(3)����NaOH��Һ��Ϊ��ͬ�������ͬŨ�ȵİ�ˮ������к���Ϊ��H1����H1�릤H�Ĺ�ϵΪ����H1_________��H(�������������=������������________________________��
�ο��𰸣�(1)���½���(���������)? Cu���ȿ죬��ֹ������ʧ
(2)-56.8 kJ��mol-1
(3)��? NH3��H2O?��������
���������(1)���ڱ�ʵ�飬���������ƺ����ᾡ���ܵ���ȫ��Ӧ�Ǽ�С����һ�����棬����ʵ��ʱ�û��β��������½������Է����¶ȼ������ñ��¹����Ǽ�С������һ����Ҫ���档����ѡ�ò�������������ͭ˿��
(2)��H=-��100 g��4.18��10-3kJ��( g����)-1��3.4 ��ݡ�0.025 mol="-56.8" kJ��mol-1
(3)��������ʵĵ�����������ȵģ���NaOH��Һ��Ϊ��ͬ�������ͬŨ�ȵİ�ˮ��Ӧ��ų��������٣����Ԧ�H1����H��
�����Ѷȣ�һ��
2��ѡ���� ��֪�Ȼ�ѧ����ʽ��
�� C2H2(g) +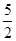 O2(g) ="=" 2CO2(g)��H2O(l)? ��H1��-1301.0 kJ?mol-1
O2(g) ="=" 2CO2(g)��H2O(l)? ��H1��-1301.0 kJ?mol-1
�� C(s)+ O2(g) ="=" CO2(g)?��H2��-393.5 kJ?mol-1
�� H2(g)+ O2(g) ="=" H2O(1)?��H3 =" -285.8" kJ��mol-1
��Ӧ�� 2C(s)+ H2(g) ="=" C2H2(g)�ġ�HΪ
A��+228.2 kJ��mol-1
B��-228.2 kJ��mol-1
C��+1301.0 kJ��mol-1
D��+621.7 kJ��mol-1
�ο��𰸣�A
��������������˹���ɵ�Ӧ�á�������֪��Ӧ��֪���ڡ�2���ۣ��ټ��õ��ܣ����Է�Ӧ���ǣ�393.5 kJ?mol-1��2��285.8 kJ��mol-1��1301.0 kJ?mol-1����228.2 kJ��mol-1����ѡA��
�����Ѷȣ���
3������� (6��)������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa�£�1g�Ҵ�ȼ������CO2��Һ̬ˮʱ����29.7kJ�����ʾ�Ҵ�ȼ���ȵ��Ȼ�ѧ����ʽΪ_____________________________��
��2����������N2��O2��ȫ��Ӧ��ÿ����23g NO2��Ҫ����16.95kJ��
��_________________________________��
��3����֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ________________________________
�ο��𰸣�(6��)��1��C2H5OH(l)+3 O2(g)=2CO2(g)+3H2O(l)?��H���C1366.8kJ��mol��1
��2��N2(g)+2O2(g) ="==" 2NO2(g)?��H��+67.8kJ��mol��1
��3��N2(g)+3H2(g) ="==" 2NH3(g)?��H����92kJ��mol��1
�����������1��ȼ������ָ��һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų�����������������1mol�Ҵ���ȫȼ�շų���������29.7kJ��46��1366.8kJ�������Ȼ�ѧ����ʽΪC2H5OH(l)+3 O2(g)=2CO2(g)+3H2O(l)?��H���C1366.8kJ��mol��1��
��2��23g NO2��Ҫ����16.95kJ������������2molNO2������16.95kJ��4��67.8kJ�������Ȼ�ѧ����ʽΪN2(g)+2O2(g) ="==" 2NO2(g)��
��3����Ӧ���Ƕϼ����յ��������γɻ�ѧ�����ų��������IJ�ֵ����Ӧ����436kJ��mol��1��3��946kJ��mol��1��391kJ��mol��1��3��2����92kJ��mol��1������Ȼ�ѧ����ʽΪN2(g)+3H2(g) ="==" 2NH3(g)?��H����92kJ��mol��1��
�����Ѷȣ�һ��
4��ѡ���� ��֪��ӦX+Y= M+NΪ���ȷ�Ӧ���������Ӧ������˵������ȷ���ǣ�?��
A��X������һ������M�ģ�Y������һ������N��
B����Ϊ�÷�ӦΪ���ȷ�Ӧ����һ��Ҫ���ȷ�Ӧ���ܽ���
C���û�ѧ��Ӧ����ʱ��ֻ�����������գ���Ϊ���ȷ�Ӧ
D��X��Y��������һ������M��N��������
�ο��𰸣�D
�����������ν���ȷ�Ӧ���Ƿ�Ӧ������������ڲ������������
�����Ѷȣ���
5��ѡ���� �ͷŻ����������ǻ�ѧ��Ӧ�������仯����Ҫ��ʽ֮һ���������й�˵������ȷ����
A���������������������ķ�Ӧ��������������ȼ�ϵ�ȼ�յȶ��Ƿ�Ӧ��ЧӦ����ҪӦ��
B����Դ�ǿ����ṩ��������Ȼ��Դ��������ʯȼ�ϡ����⡢��������ˮ����ϫ��
C��һ����ѧ��Ӧ�������������Ƿų�������ȡ���ڷ�Ӧ��������������������������Դ�С
D���ڻ�ѧ��Ӧ�����У�ֻҪ��Ӧ��������������ͬ�¶ȣ���Ӧ�����ջ�ų��������ͳ�Ϊ��ѧ��Ӧ���ʱ�
�ο��𰸣�D
���������������ͷ�Ӧ�����ֵ�����ʱ䣬����ѡ��D�Ǵ���ģ��������ȷ�ġ�����D��
�����Ѷȣ���