1��ѡ���� һ��ԭ��ص��ܷ�Ӧ����ʽΪZn��Cu2+==Zn2+��Cu����ԭ��ؿ���Ϊ
?
| A
| B
| C
| D
|
����
| Cu
| Al
| Zn
| Fe
|
����
| Zn
| Zn
| Cu
| Zn
|
�������Һ
| H2SO4
| CuSO4
| ZnCl2
| CuCl2
�ο��𰸣�D
���������
��ȷ�𰸣�D
A��Zn��2H��=Zn2����H2��
B��Al������
C�������
D����ȷ��п��o��������
�����Ѷȣ���
2��ѡ���� �����й�ԭ��ص���������ȷ����?��?��
A���ѵ���ת��Ϊ��ѧ�ܵ�װ��
B�����ý����������������ý�����ǽ���������
C�� ���·�е��ӴӸ����������� ���·�е��ӴӸ�����������
D����������������Ӧ
�ο��𰸣�C
�����������
�����Ѷȣ���
3������� ��ͼ��һ����ѧ���̵�ʾ��ͼ����֪�׳ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH�T2K2CO3+6H2O
��1���׳���______װ�ã�ͨ��CH3OH�ĵ缫������______��B�缫��������______��
��2��ͨO2һ���ĵ缫��ӦʽΪ______��
��3���ҳ����ܷ�Ӧ�Ļ�ѧ����ʽΪ______��
��4�����ҳ���A��Fe��������������6.4gʱ���׳�������O2______mL������£�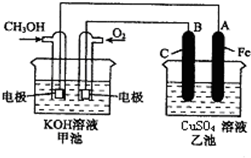
�ο��𰸣���1�����ݷ�Ӧ����ʽ֪����װ����һ��ȼ�ϵ�أ����Լ��ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã���ԭ��أ�������ӵ�Դ�������ǵ��أ�����2CH3OH+3O2+4KOH=2K2CO3+6H2O֪��CH3OH����������Ӧ�����Ըõ缫�Ǹ�����O2 ������ԭ��Ӧ�����Ըõ缫��������ʯī��ԭ��ص���������������ʯī�缫B��������
�ʴ�Ϊ��ԭ��أ�������������
��2������2CH3OH+3O2+4KOH=2K2CO3+6H2O֪��CH3OH����������Ӧ�����Ըõ缫�Ǹ�����O2 �õ��Ӻ�ˮ��Ӧ�������������ӣ�������ԭ��Ӧ�����Ըõ缫��������
�ʴ�Ϊ��O2+2H2O+4e-=4OH-��
��3���ҳ������ӷŵ�˳��Ϊ�������� Cu2+��H+��������OH-��SO42-������������ԭ��Ӧ�ĵ����غ㣬��Ϸ�Ӧ��������д��ѧ����ʽ��2CuSO4+2H2O?ͨ��?.?2Cu��+O2��+2H2SO4
�ʴ�Ϊ��2CuSO4+2H2O?ͨ��?.?2Cu��+O2��+2H2SO4��
��4�����ݵ�ʧ��������ȣ����������Ĺ�ϵʽΪ��
O2--------2Cu
22.4L? �� 2��64 ��g
1.12L?6.40g
�ʴ�Ϊ��1120��
���������
�����Ѷȣ���
4��ѡ���� �����йص�ص�˵���������
A���ֻ����õ�����ӵ�����ڶ��ε��
B��Ǧ�����и���ΪǦ�������������
C������ȼ�ϵ���������������������������
D��п�̸ɵ�ؼ�ʹ���ã����÷���Ҳ��ʧЧ
|
�ο��𰸣�C
�������������ӵ�ؿ��Է�����ŵ磬���ڶ��ε�أ�A��ȷ��Ǧ�����и���ΪǦ�������Ƕ�����Ǧ������������ᣬB��ȷ��ԭ����и���ʧȥ���ӣ������õ����ӡ�������ȼ�ϵ�����������������������������C����ȷ���ɵ���еĵ������Һ����п��Ӧ��С����ʵ����͵缫���ϵ���������п�̸ɵ�ؼ�ʹ���ã����÷���Ҳ��ʧЧ��D��ȷ����ѡC��
���㣺���鳣����ص��ж�
���������������ϵ����ʵ�ʣ�������ǿ���ѶȲ��������ڵ���ѧ����ѧϰ��Ȥ������ѧ����ѧϰ�����ԡ�
�����Ѷȣ�һ��
5��ѡ���� ����װ����ʾ��ʵ���У��ܴﵽʵ��Ŀ���ǣ�������
A��
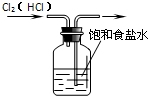
��ȥCl2�е�HCl����
B��
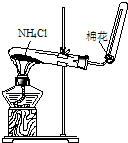
ʵ������ȡNH3
C��
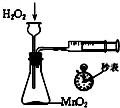
�����ⶨH2O2�ֽ⻯ѧ��Ӧ����
D��
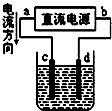
cΪ��ͭ��dΪ��ͭ����ҺΪ����ͭ��Һ����⾫��ͭ
�ο��𰸣�D
���������
�����Ѷȣ�һ��