1、简答题 某一反应体系中存在以下五种物质:Na3AsO3、H2O、I2、Na3AsO4、HI
(1)若水是产物,试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目:______;
(2)当pH为5~9时,该反应体系中的氧化反应为由HI→I2;当pH<4时,反应向逆反应方向进行,此时体系中的氧化反应为由______→______.如果两种情况下反应中转移电子数相等,则两个反应中氧化剂的物质的量之比是______;
(3)物质的氧化性和还原性不仅与溶液的酸碱性有关,还与物质的浓度和反应温度等因素有关.下列各组物质由于浓度不同而发生不同氧化还原反应的是(填序号)______.
①Cu与HNO3溶液?②Cu与FeCl3溶液?③Fe与HCl溶液?④Zn与H2SO4溶液.
参考答案:(1)当元素处于最高价时只有氧化性,所以Na3AsO4在反应中做氧化剂,对应的产物为Na3AsO3,当元素处于最低价时只有还原性,所以HI在反应中做还原剂,对应的产物为I2,故答案为:
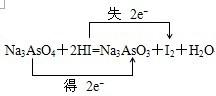
;
(2)当pH<4时,反应从I2→HI,碘元素发生了还原反应,转移电子数目为2mol,则另一个半反应应该是发生了还原反应,即为Na3AsO3→Na3AsO4,转移电子数目为2mol,所以两情况下反应中氧化剂的物质的量之比是1:1,故答案为:Na3AsO3;?Na3AsO4;1:1;
(3)①硝酸是氧化性的酸,铜和浓硝酸反应产生NO2,和稀硝酸反应产生NO,产物和硝酸浓度有关,故①正确;
②铜和三价铁反应只有一种结果生成亚铁和铜离子,和浓度无关,故②错误;
③盐酸是非氧化性的酸,和铁反应生成亚铁盐和氢气,和盐酸浓度无关,故③错误;
④稀硫酸和金属锌反应产生氢气,和浓硫酸反应生成二氧化硫,产物和硫酸浓度有关,故④正确.
故答案为:①④.
本题解析:
本题难度:一般
2、实验题 (共12分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的浓度, 请填写下列空白:
(1)将10.00 mL过氧化氢溶液至250mL ___________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数和化学式分别填在下列横线和括号内。
MnO4- + H2O2 + H+ ="=" Mn2+ + O2 + ( )
(3)移取10mL过氧化氢溶液可以用_________________(填“酸式”或“碱式”)滴定管。不用碱式滴定管盛装KMnO4标准液的原因是 ,滴定到达终点的现象是__________ _____________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的浓度为_________________________________。
(5)若盛装高锰酸钾标准溶液的滴定管用蒸馏水洗后没有用标准液润洗,则测定结果_________(填“偏高”或“偏低”或“不变”)。
参考答案:(1)容量瓶(1分)(2)2MnO4- + 5H2O2 + 6H+ = 2Mn2+ + 5O2↑+8H2O(分子式1分,配平2分,共3分)
(3)酸式 (1分) 高锰酸钾具有强氧化性,会使橡皮管老化 (2分)溶液由无色变为紫红色,且半分钟内不褪色(2分) (4) 2.5cv(2分) (5)偏高(2分)
本题解析:(1)准确配制一定体积一定物质的量浓的溶液用容量瓶,故答案为:容量瓶;(2)方程式中,高锰酸钾有强氧化性,能将双氧水氧化为氧气,先确定缺的是O2,锰元素化合价降低了5价,生成1mol氧气时,氧元素化合价升高2价,根据电子转移守恒,配平化学方程式高锰酸根前面的系数为2,双氧水前面的系数为5,根据原子守恒来配平其他物质前面的系数,2MnO4- + 5H2O2 + 6H+ = 2Mn2+ + 5O2↑+8H2O。(3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管,滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色,故答案为:酸式;滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色。(4)根据化学方程式可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol。(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。
考点:探究物质的组成或测量物质的含量;氧化还原反应方程式的配平
本题难度:一般
3、填空题 氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)配平离子方程式:______MnO4-+______HSO3-+______H+--______Mn2++______SO42-+______H2O
(2)滴定过程中,NaHSO3溶液的体积是20.00mL,消耗0.100mol/L的酸性KMnO4溶液16.00mL,则NaHSO3溶液的物质的量浓度是______?mol/L.
参考答案:(1)1mol高锰酸根离子参加氧化还原反应得到5mol电子,1mol亚硫酸氢根离子参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是10,则高锰酸根离子的计量数是2,亚硫酸氢根离子的计量数是5,其它原子根据原子守恒来配平,所以该方程式为:2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O.
故答案为:2;5;1;2;5;3.
(2)设亚硫酸氢钠的物质的量浓度为xmol/L.
2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O.
2mol? 5mol
0.0016mol? 0.02Cmol
C=O.2
故答案为:0.2.
本题解析:
本题难度:一般
4、选择题 某金属和硝酸反应,已知参加反应的被还原的硝酸和参加反应的硝酸的物质的量之比为1∶6,若已知还原产物唯一,则还原产物为
A.N2
B.N2O
C.NO
D.NO2
参考答案:A
本题解析:一般的讲,常见的金属的化合价由+1、+2、+3三种情况。当金属和硝酸反应时,二者得失电子数目一定相等。由题意知,设参加反应的被还原的硝酸的物质的量为1mol,未被还原的硝酸的物质的量为5mol,不管生成金属离子是多少价,金属失电子数=5mol,设硝酸的还原产物中氮元素的化合价为x,则氮元素得电子数目=1×(5-x)。因此有:5=1×(5-x),x=0。所以还原产物为N2,故选A。
本题难度:一般
5、选择题 将a g纯铜片投入足量的一定浓度的硝酸溶液中,反应中消耗的HNO3为b g.若a∶b=8∶21,则反应中起酸性作用的硝酸的质量为( )。
参考答案:D
本题解析:ag铜是a/64mol,则生成硝酸铜是a/64mol,所以反应中起酸性作用的硝酸的质量是a/64mol×2×63g/mol=63a/32g。又因为a∶b=8∶21,63a/32g=3b/4g,答案选D。
本题难度:一般