1、简答题 (14分)硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
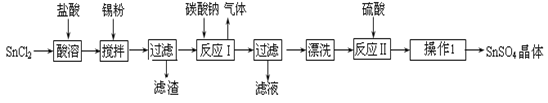
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡, Sn相对原子质量为119
回答下列问题:
(1)锡原子的核电荷数为50,锡元素在周期表中的位置是 。
(2)操作Ⅰ是 。
(3)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 。
(4)加入Sn粉的作用有两个:①调节溶液pH ② 。
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是 。
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl===SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2 + K2Cr2O7 + 14HCl ===6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1.226 g锡粉,经上述各步反应后,共用去0.100 mol/L K2Cr2O7溶液32.0ml。锡粉中锡的质量分数是 。
参考答案:(1)五周期ⅣA族
(2)加热浓缩、冷却结晶、过滤、洗涤
(3)Sn Cl2 + H2O  Sn(OH)Cl + HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
Sn(OH)Cl + HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
(4)防止Sn2+被氧化 (5)Sn2+ + CO32- ===SnO↓ + CO2↑
(6)Sn2+ + H2O2 +2H+ ="==" Sn4+ + 2H2O
(7)93.2%
本题解析:(1)Sn核电荷数为50,则:50-2-8-8-18=14,故Sn处于第五周期,ⅣA族; (2)从溶液中得到晶体的实验操作:蒸发浓缩、冷却结晶、过滤洗涤;(3)由信息可知,SnCl2可水解SnCl2+H2O?Sn(OH)Cl+HCl,盐酸浓度增大,平衡向左移动,从而抑制Sn2+水解;(4)因为Sn2+易被氧化,所以加入Sn粉除调节溶液pH外,还可防止Sn2+被氧化;(5)加入Na2CO3得到沉淀SnO,Sn元素化合价无变化,可知反应Ⅰ属于非氧化还原反应,因此所得气体为CO2,离子方程式为:Sn2++CO32-
本题难度:困难
2、选择题 FeS与一定浓度HNO3反应,生成Fe2(SO4)3.Fe(NO3)3.NO2.NO和H2O,当NO2和NO的体积为1∶1时实际参加反应的FeS与HNO3的物质的量之比是(?)
A.4∶9
B.2∶9
C.2∶11
D.1∶7
参考答案:C
本题解析:略
本题难度:一般
3、填空题 高锰酸钾(KMnO4)是一种常用的氧化剂。
(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写出该反应的离子方程式: 。
(2)高锰酸钾可代替二氧化锰用来制取Cl2,则反应中氧化剂和还原剂的物质的量之比为 。
(3)高锰酸钾与硫化亚铁有如下反应:10FeS+6KMnO4+24H2SO4=3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O。若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生转移的电子数目为 。
参考答案:(1)2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
(2)1∶5 (3)0.15NA(或9.03×1022)
本题解析:(1)MnO4-→Mn2+为还原过程,故与之对应的应为氧化过程C2O42-→CO2。根据得失电子守恒将方程式配平即可。(2)酸性条件下,KMnO4溶液的氧化性较强,其与浓盐酸反应时,被还原为Mn2+,根据电子守恒可知氧化剂和还原剂(HCl)物质的量之比为1∶5。(3)根据方程式可得关系式:
10FeS ~ 10S ~ Δm ~ e-
880 g 320 g 560 g 30 mol
2.8 g n(e-)
n(e-)=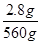 ×30 mol=0.15 mol。
×30 mol=0.15 mol。
本题难度:一般
4、填空题 (8分)单质铁溶于一定浓度的硝酸中反应的化学方程式如下:
a Fe+b NO3-+c H+="=d" Fe2++f Fe3++g NO↑+h N2O↑+k H2O(化学计量数均为正整数)
请你用已掌握的知识研究出下列规律。
(1) c、g、h的关系式是____________________。
(2) b、c、d、f的关系式是_________________________。
(3) d、f、g、h的关系式是_________________。
(4)若a =12,铁和硝酸恰好完全反应,则b的取值范围是________________。c的取值范围是______________________。
参考答案:(1) c =" 4g+10h?" (2) c-b="2d" +3f? (3) 2d +3f ="3g+8h?" (4) 6<b<12? 30<c<48
本题解析:(1)元素守恒:c="2k?" 3b="g+h+k?" 即:6b="2g+2h+c" 又:b="g+2h?" 故:c = 4g+10h
(2)电荷守恒:c="2d+3f+b?" 即:c-b=2d+3f
(3)电子转移守恒;3g+8h="2d+3f"
(4)当Fe→Fe2+,NO3-→N2O时,b有最小值。b=12×2/4 = 6
当Fe→Fe3+,NO3-→NO时,b有最大值。b=12×3/3 =" 12?" 故有:6<b<12
把6<b<12代入c=2d+3f+b(c=2d+b;c=3f+b)得:30<c<48
本题难度:一般
5、选择题 一定体积0.01 mol・L-1的稀硝酸恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01 mol・L-1 NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸的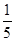 ,则样品中铁、铝的物质的量之比为( )。
,则样品中铁、铝的物质的量之比为( )。
A.2∶3
B.1∶3
C.1∶4
D.5∶3
参考答案:C
本题解析:设样品中铁和铝的物质的量分别为x和y,根据Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O、Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,反应中消耗HNO3的物质的量为4x+4y;而2Al+2NaOH+2H2O=2Na[Al(OH)4]+3H2↑中消耗NaOH的物质的量为y,即 =
=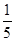 ,解得x∶y=1∶4。
,解得x∶y=1∶4。
本题难度:一般