1、填空题 某元素的原子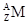 ,它的氯化物(MCl)1.17g溶于水形成的溶液,加入1mol/LAgNO3溶20ml恰好完全反应,若这种原子核内有12个中子
,它的氯化物(MCl)1.17g溶于水形成的溶液,加入1mol/LAgNO3溶20ml恰好完全反应,若这种原子核内有12个中子
则①Z和A的值是:??,?。
②请写出M元素最高价氧化物对应的水化物和与Cl元素最高价氧化物对应水化物的反应的化学方程式???。
③把M的单质放入某液体中,该液体由分子构成(每个分子有三个原子核,共有十个电子)请写出有关的反应的离子方程式??。
参考答案:①11、23
②NaOH+HClO4=NaClO4+H2O
③2Na+2H2O=2Na++2OH-+H2↑
本题解析:①根据反应Ag++Cl-=AgCl↓可知,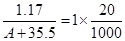 ,A=23;由于该原子核内有12个中子,则Z为11
,A=23;由于该原子核内有12个中子,则Z为11
②M元素最高价氧化物对应的水化物为NaOH,Cl元素最高价氧化物对应水化物为HClO4,两物质酸碱中和反应为NaOH+HClO4=NaClO4+H2O
③三原子核的十电子中性微粒、常温下为液体的物质为水,则钠与水反应为:2Na+2H2O=2Na++2OH-+H2↑
本题难度:简单
2、选择题 X元素的阳离子和Y元素的阴离子具有与氖原子相同的电子层结构,下列说法正确的是
A.原子序数X<Y
B.原子半径X>Y
C.原子的最外层电子数X>Y
D.元素的最高正价X<Y
参考答案:B
本题解析:X元素的阳离子和Y元素的阴离子具有与氖原子相同的电子层结构,则X一定是第三周期的金属元素,Y一定是第二周期的非金属元素,所以原子序数是X>,原子半径X>Y,最外层电子数是X<Y,但元素的最高正价不一定是X<Y,例如F没有正价,所以正确的答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑推理能力,易错点是学习D。
本题难度:一般
3、选择题 在d轨道中电子排布成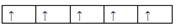 ,而不排成
,而不排成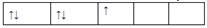 最直接的根据是? (? )
最直接的根据是? (? )
A.能量最低原理
B.泡利不相容原理
C.洪特规则的特例
D.洪特规则
参考答案:D
本题解析:洪特规则是在同一亚层中的电子尽可能分占不同轨道,而且自旋方向相同。
本题难度:一般
4、填空题 不能说明氧元素比硫元素非金属性强的事实是
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
参考答案:C
本题解析:A中利用的是原子的得电子能力越强,即元素的非金属性越强,则气态氢化物越稳定;B中2H2S+O2=2S+2H2O,则氧化性:O2>S,单质的氧化性越强,说明原子的得电子能力越强,即元素的非金属性越强;D中O2将Cu氧化到+2价,S将Cu氧化到+1价,说明氧化性:O2>S,单质的氧化性越强,说明原子的得电子能力越强,即元素的非金属性越强;
本题难度:一般
5、选择题 下列元素中价电子排布不正确的是( )
A.V:3d34s2
B.Cr:3d44s2
C.Ar:3s23p6
D.Ni:3d84s2
参考答案:B
本题解析:随着原子核外电子层数的增多,核外电子排布出现能级交错现象,如3d能量高于4s,所以按照构造原理排布时,就要先排满4s,再排3d。此外还要注意:当轨道全充满(s2、p6、d10)、半充满(s1、p3、d5)或全空(p0、d0)时更稳定,所以B中元素Cr的价电子排布应为3d54s1。错因:对轨道全充满、半充满等是原子的稳定状态理解不准。与Cr相似的还有Cu,其价电子排布为3d104s1,而不是3d94s2。
本题难度:一般