1、填空题 已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验
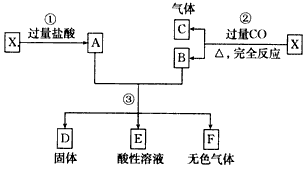
(1)写出①、②和③步所有反应的化学方程式:①________; ②________;③________
(2)设从③步所得固体D的质量为32g,溶液E中只含有一种金属离子,气体F在标准状况下体积为5.6 L,试计算取用的每份X的质量_________和X中FeO与CuO的质量比____________。
参考答案:
(l)①FeO+2HCl=FeCl2+H2O、CuO+2HCl=CuCl2+H2O;②FeO+CO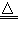 Fe+CO2、CuO+CO
Fe+CO2、CuO+CO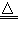 Cu+CO2;
Cu+CO2;
③CuCl2+Fe=Cu+FeCl2、Fe+2HCl=FeCl2+H2↑
(2)56g;m(FeO):m(CuO)=9:5
本题解析:
本题难度:一般
2、实验题 (共14分)A、B、C为3种单质(其中A为固体,B、C为气体),D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E。它们之间的转化关系如下图:
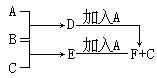
填写下列空白:
(1)(3分)物质A是?,B是?,B的离子结构示意图为?。
(2)(5分)写出化合物E的电子式:?,D的饱和溶液滴入沸水中溶液呈红褐色的原因是(用离子方程式表示):?。D溶液可以用来止血,请简单说明其止血原理是:?。
(3)(4分)工业上把B单质与石灰乳反应可制得漂白粉,漂白粉的有效成份是?,漂白粉常用于自来水的杀菌消毒,原因是(写出反应的化学方程式,并加以适当的文字
说明):?。
(4)(2分)F中加入NaOH溶液,并在空气中放置由白色变为灰绿色最后变成红褐色沉淀的化学方程式是?。
参考答案:(1) Fe 、 Cl2 ?、?略? ( 3分)
(2) 略? (1分)、? Fe3+ + 3H2O 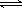 ?Fe(OH)3 + 3H+ ?(2分)
?Fe(OH)3 + 3H+ ?(2分)
血液本质上是一种液溶胶,而三氯化铁是电解质,大量电解质溶液一遇到血液这种溶胶就会使血液迅速发生聚沉,生成的沉淀会堵塞伤口从而达到止血的效果. (2分)
(3)Ca(ClO)2 (1分) 、 Ca(ClO)2 + CO2 +H2O = CaCO3 + 2HClO? (2分)
自来水中的次氯酸钙与空气中的CO2反应后生成了次氯酸,次氯酸有强氧化性,能起杀菌消毒作用。(1分)
(4)、4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 (2分)
本题解析:略
本题难度:一般
3、推断题 已知A是短周期非金属元素形成的单质,B是某纯净物或其溶液,二者之间的反应可表示为:A+B→C +D(若生成物有三种且有水时,水被略去)。
(1)若该反应在常温下能剧烈发生,C、D中有一种物质的溶液能腐蚀玻璃,则反应的化学方程式可表示为________________
(2)若A、C、D均含有氧元素,且这三种物质混合后能形成一种新物质E,B与E能发生化合反应生成盐F,则F中含有的化学键类型有____________,F中阴、阳离子的电子数之比为________________。
(3)若A为固体,B为碱溶液,C与D在酸性条件下又能转化为A,则A与B反应的离子方程式为________________________。
(4)若A、B、C均为固体,D为气体。写出两个满足此条件的化学方程式:____________、 ____________
参考答案:(1)2F2+2H2O=4HF+O2
(2)离子键、共价键;16:5
(3)3S+6OH-=2S2- + SO32-+3H2O (4)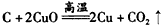 ;
;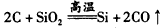
本题解析:
本题难度:一般
4、简答题 现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.

填写下列空白:
(1)A中含单质为为______写化学式)
(2)写出A中的某一单质与烧碱溶液反应的离子方程式______
(3)写出固体F与硝酸反应的化学方程式,并标出电子转移的方向和数目______
(4)将F与浓硝酸反应产生的气体依次通过足量的碳酸氢钠溶液、浓硫酸、足量Na2O2固体、水最终得到的气体与原气体的体积比为______.
参考答案:合金与氢氧化钠溶液反应,生成无色可燃气体B,B为H2,合金可能含有Al、Si;
合金与氢氧化钠溶液反应,得到的无色溶液C,C中加入盐酸生成白色沉淀E,沉淀E加入过量盐酸,有白色固体,该白色固体为H2SiO3,向加入过量盐酸得到无色溶液中加过量氨水,生成白色沉淀,该白色沉淀为Al(OH)3,故合金含有Si、Al,白色沉淀E为H2SiO3、Al(OH)3;
固体D加入盐酸生成氢气与浅绿色溶液,浅绿色溶液中加入漂白粉,生成红褐色沉淀,为Fe(OH)3,故D中含有铁,即合金中含有铁;
固体D加入盐酸后过滤得到不溶物F,F燃烧生成无色、无刺激性的气体G,与浓硝酸反应生成红棕色气体NO2,F为碳符合转化关系与题意,G为CO2,故合金中含有碳单质,
(1)综合上述分析可知,A中含单质为:Al、Si、C、Fe;
故答案为:Al、Si、C、Fe;
(2)Al与Si都能与氢氧化钠溶液发生离子反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑或Si+2OH-+H2O=SiO32-+2H2↑;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑或Si+2OH-+H2O=SiO32-+2H2↑;
(3)固体C与浓硝酸反应的化学方程式的方程式为:C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O,反应中电子转移数目为4,标出电子转移的方向和数目为:
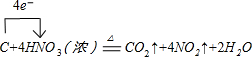
;
故答案为:
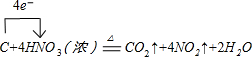
;
(4)固体C与浓硝酸反应的化学方程式的方程式为:C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O,假定生成CO2为1mol、NO2为4mol,产生的气体依次通过足量的碳酸氢钠溶液,发生反应3NO2+H2O=2HNO3+NO,生成83molHNO3,43molNO,同时发生HNO3+NaHCO3=CO2↑+H2O,83molHNO3可以生成83molCO2,故出来气体中:CO2为1mol+83mol=113mol,NO为43mol,及水蒸气.通过浓硫酸水被吸收,再通过足量Na2O2固体发生反应2Na2O2+2CO2=2Na2CO3+O2,113molCO2生成116molO2,再发生2NO+O2=2NO2,43molNO,消耗23molO2,剩余O2为116mol-23mol=76mol,生成NO243mol,最后发生反应4NO2+O2+2H2O=4HNO3,43molNO2消耗13molO2,最后剩余O2为76mol-13mol=56mol,故最终得到的气体与原气体的体积比为56mol:(1mol+4mol)=1:6;
故答案为:1:6.
本题解析:
本题难度:一般
5、推断题 已知A为一无机盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。?

(1)写出G的电子式_______________,M的化学式_____________;
(2)写出反应②的离子反应方程式______________________________;
(3)写出反应③的化学反应方程式________________________;反应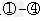 中属于非氧化还原反应的是_________?;
中属于非氧化还原反应的是_________?;
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极_______________________ 阳极____________________
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:F=1:2:2:2:2,写出A分解的反应方程式______________________
参考答案:(1)?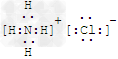 ?;?KSCN?
?;?KSCN?
(2)3Fe2+ +NO3-+4H+=?3Fe3+ +NO↑+2H2O?
(3)4NH3+3O2=2N2+6H2O?;①④?
(4)阴极:Fe3+ +e-=?Fe2+?;?阳极:2Cl-?-?2e-=?Cl2?↑?
(5)(NH4)?2Fe(C2O4)2=FeO+2CO↑+2CO2↑+2H2O+2NH3?↑
本题解析:
本题难度:一般