1��ѡ���� X��Y��Z�������壬ȡX��Y��1��1�����ʵ���֮�Ȼ�ϣ������ܱ������з������·�Ӧ��X+2Y?2Z���ﵽƽ���û�������з�Ӧ��������ʵ�����������������ʵ���֮��Ϊ3��2����Y��ת������ӽ��ڣ�������
A��35%
B��40%
C��50%
D��65%
�ο��𰸣�����X��Y���ʵ���Ϊ1mol����ƽ��ʱ����Y���ʵ���Ϊm���������������ʽ����
? ? X+2Y?2Z
��ʼ����mol��? 1? 1? 0?
�仯����mol��? 0.5m? m? m
ƽ������mol�� 1-0.5m?1-m?m
ƽ���û�������з�Ӧ��������ʵ��������������ʵ���֮��Ϊ3��2����
��1-0.5m+1-m����m=3��2
? m=23
Y��ת����=231��100%=67%
��ѡD��
���������
�����Ѷȣ�һ��
2�������� ��6�֣���500���ݻ�Ϊ2�����ܱ������г���SO2��O2������SO2��Ũ��Ϊ1mol/L����10��ﵽƽ�⣬2SO2(g)+O2(g) 2SO3(g)����ʱ������SO3��Ũ��Ϊ0.9mol/L��O2�����ʵ���Ϊ2.1mol������ SO2��ת���ʣ��� O2����ʼŨ��(mol/L)���� SO2��ƽ����Ӧ����(mol/L�� min)
2SO3(g)����ʱ������SO3��Ũ��Ϊ0.9mol/L��O2�����ʵ���Ϊ2.1mol������ SO2��ת���ʣ��� O2����ʼŨ��(mol/L)���� SO2��ƽ����Ӧ����(mol/L�� min)
�ο��𰸣���90%? ��1.5mol /L? �� 5.4 mol/L�� min
���������2SO2?+? O2? ?2SO3
?2SO3
ʼc:? 1? 1.5? 0
��c:? 0.9? 0.45? 0.9
ƽc:? 0.1? 1.05? 0.9
V(SO2)=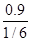 ="5.4" mol/L�� min
="5.4" mol/L�� min
�����Ѷȣ�һ��
3������� ��10�֣���¯���������з�������Ҫ��ӦΪ��1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
�¶�/��
| 1000
| 1150
| 1300
|
ƽ�ⳣ��
| 4.0
| 3.7
| 3.5
|
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
��ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK=?����H?0(�>������<����=��)��
(2)��һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0 mol����Ӧ����l0 min��ﵽƽ�⡣���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ���ʦ�(CO2)=?��CO��ƽ��ת����= ?��
(3)�����(2)��CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��?��
A������Fe����? B������Fe2O3����? C���Ƴ�����CO2
D����߷�Ӧ�¶�? E����С�������ݻ�? F��������ʵĴ���
�ο��𰸣���c(CO2)/ c(CO)��2�֣�����2�֣�
��6��10��3mol/(L��min)(2��)? 60%��2�֣�? ��c��2�֣�
�����������1��ƽ�ⳣ����ָ��һ�������µĿ��淴Ӧ�У����ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ���ѵõ���֮���ı�ֵ�����������ʽΪK��c(CO2)/ c(CO)�������й����ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС�����������¶ȣ�ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ��
��2����ƽ��ʱCO�����ʵ���Ũ����x��������CO��Ũ����0.1��x������CO2Ҳ��0.1��x��ƽ����CO2����0.1��x��0.1��0.2��x������ƽ�ⳣ����֪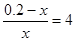 ?�����x��0.04mol/L����������CO��0.1mol/L��0.04mol/L��0.06mol/L������ת������0.06��0.1��1005=60%��CO2�ķ�Ӧ������0.06mol/L��10min��6��10��3mol/(L��min)��
?�����x��0.04mol/L����������CO��0.1mol/L��0.04mol/L��0.06mol/L������ת������0.06��0.1��1005=60%��CO2�ķ�Ӧ������0.06mol/L��10min��6��10��3mol/(L��min)��
��3�����������ı仯����Ӱ��ƽ��״̬��AB����ȷ��C�ǽ��������Ũ�ȣ�ƽ��������Ӧ�����ƶ���ת������������Ӧ���ȣ������¶�ƽ�����淴Ӧ�����ƶ���ת���ʽ��͡���Ӧǰ��������䣬�ı�ѹǿ��ƽ�ⲻ�ƶ���ͬ������Ҳ����Ӱ��ƽ��״̬��������ȷ�Ĵ���C��
�����Ѷȣ�һ��
4������� ���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;�����ش��������⣺
��1�������ڸ�������ˮ������Ӧ�Ļ�ѧ����ʽΪ��CH4��H2O��CO��3H2���������ʵ�ȼ�����������±�

��֪1mol H2O(g)ת��Ϊ1mol H2O(l)ʱ�ų�44.0kJ������д��CH4��ˮ�����ڸ����·�Ӧ���Ȼ�ѧ����ʽ
_________________________��
��2��500�桢50MPaʱ�����ݻ�ΪVL�������м���1mol N2��3mol H2����ʱN2��ת����Ϊa����ƽ��ʱ
NH3��Ũ��Ϊ______________��
��3��1,3�D����������Ҫ�Ļ���ԭ�ϣ�����ϩ�ϳ�1,3�D��������·������
CH2=CH2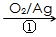
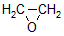
 HOCH2CH2CHO
HOCH2CH2CHO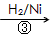 HOCH2CH2CH2OH
HOCH2CH2CH2OH
ij�������ѹ�����ϩ11.2t�����ǵ�ԭ�ϵij�����ã���Ӧ�ڡ��������CO��H2��������������Ӧ���

���������������У���Ӧ�١��ڡ����и��л����ת���ʾ�Ϊ100%���ҷ�Ӧ����CO��H2����Ӧ����H2��ת���ʶ�Ϊ80%������������Ҫ��̿___________�֡�����_________�֣���������������Ҫ��
�ο��𰸣���1��CH4(g)+H2O(g)==CO(g)+3H2(g) ��H=+206.1 kJ��mol-1
��2��2a/Vmol/L
��3��3.0t��4.0t
���������
�����Ѷȣ�һ��
5��ѡ���� ��2L�̶��ܱ������У�����1molA�����3molB���壬���¶�ΪT���½������з�Ӧ��A��g��+2B��g�� 3C��g������H��0���ﵽƽ��ʱAת����Ϊ50%���ס�������ѧС�飬�����¶�ΪT�棬�ֱ���2L�̶��ܱ������г���һ����A�����B���壮�ף�2molA��6molB���ң�1molA��6molB����¼��Ӧʱ������A�����ʵ��������ʾ������˵����ȷ���ǣ�������
3C��g������H��0���ﵽƽ��ʱAת����Ϊ50%���ס�������ѧС�飬�����¶�ΪT�棬�ֱ���2L�̶��ܱ������г���һ����A�����B���壮�ף�2molA��6molB���ң�1molA��6molB����¼��Ӧʱ������A�����ʵ��������ʾ������˵����ȷ���ǣ�������
| t/min | ����A�����ʵ��� | ����A�����ʵ���
0
2
1
5
1.0
0.5
|
A����Ӧ�ڵ�5minʱ��������v��������v���棩
B����Ӧ�ڵ�5minʱ��������3v��B����=2v��C�棩
C����Ӧ�ڵ�5minʱ���ס�����������ڻ�ѧƽ��״̬
D��ǰ5min�У�������A��ʾ�Ļ�ѧ��Ӧ����Ϊv��A��=0.2mol/��L?min��
�ο��𰸣���֪��T��ʱA��g��+2B��g�� 3C��g��
3C��g��
��ʼ��0.5mol/L 1.5mol/L 0
ת����0.25mol/L 0.5mol/L0.75mol/L
ƽ�⣺0.25mol/L 1.0mol/L 0.75mol/L
��k=0.7530.25��1��02=1.6875��
���飺T��ʱA��g��+2B��g�� 3C��g��
3C��g��
��ʼ��1mol/L3mol/L 0
ת����0.5mol/L1.0mol/L 1.5mol/L
ƽ�⣺0.5mol/L 2mol/L 1.5mol/L
���飺T��ʱA��g��+2B��g�� 3C��g��
3C��g��
��ʼ��0.5mol/L 3mol/L 0
ת����0.25mol/L0.5mol/L 0.75mol/L
ƽ�⣺0.25mol/L 2.5mol/L 0.75mol/L
�����Q��=1��530.5��22=1.6875������Q��=0.7530.25��2��52=0.27����
A����Ӧ�ڵ�5minʱ��������Q�ң�k��û�дﵽƽ��״̬����Ӧ������Ӧ���У���v��������v���棩����A����
B����Ӧ�ڵ�5minʱ������k=1.6875���ﵽƽ��״̬������3v��B����=2v��C�棩����B��ȷ��
C����Ӧ�ڵ�5minʱ������k=1.6875���ﵽƽ��״̬������Q�ң�k��û�дﵽƽ��״̬����C����
D��ǰ5min�У�������A��ʾ�Ļ�ѧ��Ӧ����Ϊv��A��=0.5mol/L5min=0.1mol/��L?min������D����
��ѡB��
���������
�����Ѷȣ�һ��