1、推断题 [三选一―选修3:物质结构与性质]
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为______、____;
(2)XZ2与YZ2分子的立体结构分别是_______和_______,相同条件下两者在水中的溶解度较大的是
___(写分子式),理由是____________;
(3)Q的元素符号是___,它属于第____周期,它的核外电子排布式为_____,在形成化合物时它的最高化合价为_______;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键___________。
参考答案:(1)S;C
(2)V形;直线形;SO2;因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大
(3)Cr;四;1s22s22p63s23p63d54s1;+6
(4) F-H…F F-H…O O-H…F O-H…O
本题解析:
本题难度:一般
2、选择题 X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻.X 的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。下列说法正确的是
[? ]
A.还原性:X的氢化物>Y的氢化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX2、M2Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
参考答案:D
本题解析:
本题难度:一般
3、简答题 某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象发如表:
| 实验方案 | 实验现象
1.用砂纸擦后的镁带与沸水反应,再向反应液中滴加酚酞
2.向新制的H2S饱和溶液中滴加新制的氯水
3.钠与滴有酚酞试液的冷水反应
4.镁带与2mol/L的盐酸反应
5.铝条与2mol/L的盐酸反应
6.向AlCl3溶液中滴加NaOH溶液至过量
A.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色
B.产生大量气体,气体可燃,溶液变浅红色
C.反应不十分强烈,产生的气体可燃
D.剧烈反应,产生的气体可燃
E.生成白色絮状沉淀,继而沉淀消失
F.生成淡黄色沉淀
|
请你帮助该同学整理并完成实验报告
(1)实验目的:______
(2)实验用品:仪器、材料______?药品______
(3)实验内容:(填写题给信息表中的序号或大写英文字母,并写出有空格处的离子方程式)
| 实验方案 | 实验现象 | 有关离子方程式
?
A
?
?
B
不? 填
?
?
不? 填
?
?
不? 填
?
E
?
?
F
?
|
(4)实验结论:______.
参考答案:(1)根据题干“某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案同周期元素金属性”结合实验内容可以确定该实验的目的是:探究同周期元素金属性、非金属性的性质递变规律,
故答案为:探究同周期元素金属性、非金属性的性质递变规律(验证Na、Mg、Al金属性强弱及S、Cl非金属性强弱);
(2)根据实验步骤可以确定所需的仪器、材料主要有:试管、酒精灯、砂纸、胶头滴管,药品有:金属钠、镁条、铝条、酚酞试液、盐酸、氯化铝溶液、氢氧化钠溶液、冷水和沸水、新制的H2S饱和溶液、氯水,
故答案为:试管、酒精灯、砂纸、胶头滴管;金属钠、镁条、铝条、酚酞试液、盐酸、氯化铝溶液、氢氧化钠溶液、冷水和沸水、新制的H2S饱和溶液、氯水;
(3)金属钠、镁、铝和水、酸反应置换出氢气是越来越难的,反应的剧烈程度是越来越弱的,据此来回答实验的现象并写出化学方程式,故答案为:
实验方案实验现象有关离子方程式3A2Na+2H2O=2Na++2OH-+H2↑1B?4?5?6EAl3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O2FH2S+Cl2=2H++2Cl-+S↓(4)同周期元素随原子序数的增大,元素的金属性逐渐减弱,而非金属逐渐增强.
本题解析:
本题难度:一般
4、选择题 下列叙述中,不正确的是
A.元素最高化合价:NaO>F
C.酸性:H3PO4D.原子核外电子层数:Li
参考答案:B
本题解析:元素周期律的相关知识考查
本题难度:一般
5、推断题 U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。 请回答下列问题:
⑴V的单质分子的结构式为_______________;XW的电子式为____________;Z元素在周期表中的位置是_____________。
⑵U元素形成的同素异形体的晶体类型可能是(填序号)__________。
① 原子晶体 ② 离子晶体 ③ 分子晶体 ④ 金属晶体
⑶U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)____________;V、W的氢化物分子结合H+能力较强的是(写化学式)______________,用一个离子方程式加以证明_________________________________________________。
⑷YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
_________________________,由此可知VW和YW2还原性较强的是(写化学式)___________。
参考答案:⑴N≡N;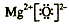 ;第4周期,第VIII族
;第4周期,第VIII族
⑵①③?
⑶CH4;NH3;NH3+H3O+==NH4++H2O
⑷3SO2+2NO3-+ 3Ba2++2H2O==3BaSO4↓+2NO+4H+;SO2
本题解析:
本题难度:一般