1、填空题 (1)下列实验操作或叙述正确的是?(填写编号,多选扣分)
①不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体;
②为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴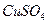 溶液;
溶液;
③用蒸馏水润湿的pH试纸测定溶液的pH一定有误差;
④向沸腾的NaOH稀溶液中滴加 饱和溶液,可以制得
饱和溶液,可以制得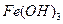 胶体;
胶体;
⑤配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑥定容时,俯视容量瓶刻度,造成所配溶液浓度偏高;
⑦称取5.85g氯化钠固体,用100 mL蒸馏水溶解,得到1.00 mol・L-1氯化钠溶液
(2)某钠盐溶液可能含有阴离子NO3-,CO32-,SO32-,SO42-,Cl-,Br-,I-。为鉴定这些离子,分别取少量溶液进行以下各步骤的实验:
步骤1测得混合液呈碱性;
步骤2滴加HCl时,溶液中出现气泡。该气体能使饱和石灰水溶液变浑浊;
 步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
步骤4加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
步骤5加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
分析上述5个实验,回答下列问题。
①由实验步骤1判断可能存在的离子有?;
②由实验步骤2判断可能存在的离子有几种可能性?;分别是?;
③由实验步骤3可得出的结论是 ?;
④由实验步骤4和实验步骤5可确定肯定存在的离子有?;
⑤由上述5个实验不能确定是否存在的离子是?。
参考答案:(1) ①②⑥?(选对1 个1 分,选对3个3分。漏选或错选1个扣1分,至为0分,不出现负分)
(2) ① CO32-或 SO32- ,CO32-和SO32-? (2分)
②有四种可能性 (2分)
CO32-?(1分)
SO32-?(1分)
CO32-?SO32-?(1分)
CO32-?SO32-?NO3- ?(1分)
③?Br-(1分)? I-不存在? (1分)
④?SO42-(1分),? Cl-? (1分)
⑤? NO3- (1分)
本题解析:略
本题难度:一般
2、实验题 某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石不含其他与CO 反应的成分),并除去尾气。CO用反应H2C2O4 = CO2↑+CO↑+H2O来制取。与Fe2O3反应的CO需纯净、干燥。

(1)若所制的气体的流向为从左向右时,下列仪器组装连接的顺序是(用a"b……表示)____接 ____,___接____,____接 ____,____接___。
(2)装置乙的作用是________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是_______________。
(4)实验前氧化铁矿粉末的质量为xg,实验后测得乙和丙的质量分别增加了yg和zg,则氧化铁矿粉末中氧化铁的质量分数为____。
参考答案:(1)a;b;c;f;g;h;l;d或a;d;e;f;g;h;i;b
(2)吸收CO2
(3)防止还原产生的Fe受热时被氧化
(4)40y/33x×100%或40z/33x×100%
本题解析:
本题难度:一般
3、实验题 某兴趣小组的同学发现,将CuSO4溶液与Na2CO3溶液混合会产生蓝绿色沉淀。他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究。
【提出猜想】
猜想1:所得沉淀为___;
猜想2:所得沉淀为___;
猜想3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2・nCuCO3]。
查阅资料获知,无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤、风干;
步骤2:取一定量所得固体,用如下装置(夹持仪器未画出)进行定性实验。
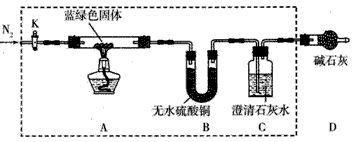
能证明猜想1成立的实验现象是____。
【问题讨论】
(1)检查上述虚线框内装置气密性的实验操作是:关闭K,____。
(2)若在上述装置B中盛放无水CaCl2,C中盛放Ba(OH)2溶液,还可测定所得沉淀的组成。
①C中盛放Ba(OH)2溶液,而不使用澄清石灰水的原因是________。
②若所取蓝绿色固体质量为27.1 g,实验结束后,装置B的质量增加2.7 g,C中产生沉淀的质量为19.7 g。则该蓝绿色固体的化学式为___。
参考答案:【提出猜想】Cu(OH)2 ;?CuCO3
【实验探究】B中白色固体变蓝,C中无明显现象(若猜想1所得沉淀为 CuCO3,则实验现象为B中无明显现象,C中产生白色沉淀)
【问题讨论】
(1)用酒精灯微热硬质玻璃管,若C中有气泡逸出,撤去酒精灯,冷却一段时间后,C中导管内形成水柱,则证明装置的气密性良好
(2)①Ba(OH)2的溶解度大于Ca(OH)2,充分吸收CO2;BaCO3的摩尔质量大于CaCO3,测量误差小;
②Cu5(OH)6(CO3)2[或3Cu(OH)2・2CuCO3]
本题解析:
本题难度:一般
4、实验题 (7分)硫酸亚铁是一种可用于治疗缺铁性贫血的药剂,硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的O2氧化成硫酸铁。请设计一种方法,验证某硫酸亚铁药品是否已被氧化。请写出主要步骤、现象及化学方程式。
参考答案:把药片刮去糖衣,用研钵研碎,在试管中用少量蒸馏水溶解,滴几滴KSCN溶液,若溶液显红色,则得知硫酸亚铁被氧化。有关化学方程式:
Fe2(SO4)3+6KSCN====2Fe(SCN)3+3K2SO4
本题解析:本题的实验设计是操作简单的试管实验。操作时要连续完成,避免在空气中放置时间过长而被氧化。
本题难度:简单
5、填空题 (16分)某兴趣小组为验证日常生活用的火柴头上只含有KClO3、MnO2、S,设计了以下实验流程图,请回答以下问题:

(1) 写出步骤①中可能发生一个反应的化学方程式?。
(2)为验证气体A,按下图所示进行实验:若能观察到?的现象,即可证明火柴头上含有S元素。
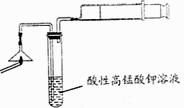
(3) 步骤②的实验操作装置如下图所示
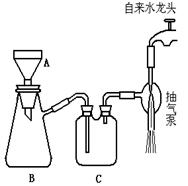
a.该操作的名称是?。
b.写出图中A仪器的名称: __?___;
c.该装置图有几处错误.
请指出
B仪器处关键性的错误:__________ C仪器处的错误改进后应是:?。
(4)要证明火柴头中含有Cl元素,
在步骤②以后的实验步骤是?。
(5)有学生提出检验火柴头上中含有Cl元素,另一套实验方案:

请写出有关的离子反应方程式为?,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是?。
参考答案:(共16分)
(1)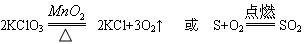 (2分)
(2分)
(2)KMnO4溶液(紫红色)褪色(2分)
(3)a.减压过滤(或抽滤)(2分)
b.A布氏漏斗;(2分)
c.布氏漏斗颈口没有朝向吸滤瓶的支管口,或布氏漏斗的颈口斜面没有与吸滤瓶的支管口相对。(1分);短进长出.(1分)
(4)取少量滤液C,加入HNO3和AgNO3溶液,若观察到白色沉淀产生,即可证明火柴头中含有氯元素。(2分)
(5)ClO3?+3NO2-+Ag+=AgCl↓+3NO3?(2分)
AgNO2与AgCl均为不溶于水的白色沉淀。或者应加HNO3溶液(2分)
本题解析:略
本题难度:简单