1��ѡ���� ���Ѵﵽƽ��Ŀ��淴Ӧ2SO2��O2 2SO3�У�������18O��ɵ�����һ��ʱ���18O���������������е�(? )
2SO3�У�������18O��ɵ�����һ��ʱ���18O���������������е�(? )
A�������������
B�����ɵ�����������
C�������Ͷ���������
D��������������������������
2��ѡ���� ij�¶��£���֪��ӦmX(g)��nY(g) qZ(g)?��H��0��m��n��q�������һ�����ܱ�������Ͷ�뷴Ӧ��ﵽƽ�⣬����������ȷ����(? )
qZ(g)?��H��0��m��n��q�������һ�����ܱ�������Ͷ�뷴Ӧ��ﵽƽ�⣬����������ȷ����(? )
A��ͨ������������ѹǿ��ƽ�������ƶ�
B���ټ���X����Ӧ���յ���������
C������Y�����ʵ�����X��ת���ʼ�С
D�������¶ȣ�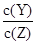 ��ֵ��С
��ֵ��С
3��ѡ���� ���з�ӦX��g��+Y��g�� 2Z��g����H<0����ͼ��ʾ�ӷ�Ӧ��ʼ��t
2Z��g����H<0����ͼ��ʾ�ӷ�Ӧ��ʼ��t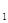 sʱ�ﵽƽ�⣬��t
sʱ�ﵽƽ�⣬��t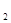 sʱ���������仯ʹƽ���ƻ�����t
sʱ���������仯ʹƽ���ƻ�����t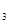 sʱ�ִ�ƽ�⡣����ͼ��t
sʱ�ִ�ƽ�⡣����ͼ��t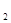 sʱ�ı������������
sʱ�ı������������

A������ѹǿ
B��ʹ���˴���
C�������¶�
D����С��X��Y��Ũ��
4������� ��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ��
��1�����á���ѧ����ת�Ʒ����Ʊ�TaS2���壬�������·�ӦTaS2(s)+2I2(g) TaI4(g)+S2(g)? ��H��0?����Ӧ����ƽ�ⳣ������ʽK=?����K=1����ij�����ܱ������м���1mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ ?��
TaI4(g)+S2(g)? ��H��0?����Ӧ����ƽ�ⳣ������ʽK=?����K=1����ij�����ܱ������м���1mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ ?��
��2����ͼ��ʾ����Ӧ������ʯӢ��չ��н��У������¶�ΪT2��һ�˷���δ�ᴿ��TaS2��ĩ������I2��g����һ��ʱ������¶�ΪT1��һ�˵õ��˴�����TaS2���壬���¶�T1?T2���������������=������������Ӧ��ϵ��ѭ��ʹ�õ�������?��
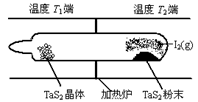
��3������I2�������Կɲⶨ��������ĺ����������ǽ������е���ת��Ϊ H2SO3��Ȼ����һ��Ũ�ȵ�I2��Һ���еζ�������ָʾ��Ϊ?���ζ���Ӧ�����ӷ���ʽΪ?��
��4��25��ʱ��H2SO3 HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh=?mol/L������NaHSO3��Һ�м���������I2������Һ��
HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh=?mol/L������NaHSO3��Һ�м���������I2������Һ��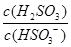 ��?���������С�����䡱����
��?���������С�����䡱����
5������� ��100��ʱ����0.100mol��N2O4�������1L��յ��ܱ������У���һ��ʱ��Ը������ڵ����ʽ��з������õ������
ʱ��/s
Ũ��mol?L-1 | 0 | 20 | 40 | 60 | 80 | 100
c��N2O4��mol?L-1
0.100
c1
0.050
c3
a
b
c��NO2��/mol?L-1
0.000
0.060
c2
0.120
0.120
0.120
|
����գ�
��1���ﵽƽ��ʱN2O4��ת����Ϊ______%������c2______c3��a______b?��ѡ�������������=������
��2��20s��������������Ũ��c1=______mol?L-1����0s��20s��������������ƽ����Ӧ����Ϊ______mol?��L?s��-1����
��3��������ͬ���������������������Ƕ�����������Ҫ�ﵽ����ͬ����ƽ��״̬��������������ʼŨ����______mol?L-1��