1、填空题 已知:2SO3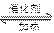 2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题:
2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题:
(1)反应达平衡所需时间A?B(大于;等于;小于);达平衡时SO3的转化率
A?B(大于;等于;小于)。
(2)若平衡后,向A、B中分别充入惰性气体,?容器的平衡将向?方向移动;若平衡后,向A、B中分别充入等物质的量SO3,重新达平衡时,两容器中的SO3转化率变化情况是(填变大、变小、不变)A?,B?
参考答案:
(1)小于;小于(各1分,共2分)
(2)B;正反应;变小;不变(各1分,共4分)
本题解析:
本题考查化学平衡移动;2SO3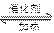 2SO2+O2,是一气体总物质的量增大的反应。(1)相同温度下,充入SO3,A容器保持体积不变,压强变大;B容器保持压强不变,体积增大,达到平衡状态时转化为状态C(如下图),故达到平衡所用时间,A小于B;假设B中的活塞不移动,由于A、B两个容器的体积、温度相同,达到平衡时A、B两容器中存在的平衡是等效平衡,其中SO3的转化率也相等。对于B和C两个状态,B中压强小于C中压强,因此C中SO3转化率大于B中SO3转化率。由此可以判断出C中SO3的转化率也大于A中SO3的转化率, 故达到平衡时,SO3的转化率 A小于B。
2SO2+O2,是一气体总物质的量增大的反应。(1)相同温度下,充入SO3,A容器保持体积不变,压强变大;B容器保持压强不变,体积增大,达到平衡状态时转化为状态C(如下图),故达到平衡所用时间,A小于B;假设B中的活塞不移动,由于A、B两个容器的体积、温度相同,达到平衡时A、B两容器中存在的平衡是等效平衡,其中SO3的转化率也相等。对于B和C两个状态,B中压强小于C中压强,因此C中SO3转化率大于B中SO3转化率。由此可以判断出C中SO3的转化率也大于A中SO3的转化率, 故达到平衡时,SO3的转化率 A小于B。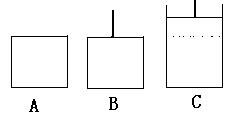
(2)达到平衡后,分别充入惰性气体,A容器体积不变,反应体系的浓度不变,平衡不移动,B容器保持压强不变,体积增大,平衡向右移动;如果充入SO3,A容器保持体积不变,压强变大,SO3的转化率减小,B中充入SO3,与原平衡为等效平衡,SO3的转化率不变。
本题难度:一般
2、填空题 (13分)难溶性杂卤石(K2SO4・MgSO4・2CaSO4・2H2O)属于“呆矿”,在水中存在如下平衡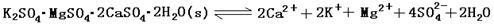
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
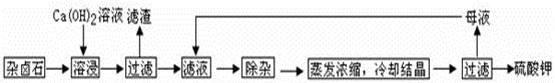
(1)滤渣主要成分有?和?以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:?。
(3)“除杂”环节中,先加入?溶液,经搅拌等操作后,过滤,再加入?溶液调滤液PH至中性。
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图14,由图可得,随着温度升高,?
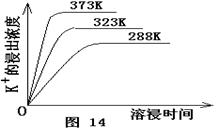
① 在相同时间K+的浸出浓度大。
② 在相同时间K+的浸出浓度减小
③ 反应的速率加快,平衡时溶浸时间短。
④ 反应速率减慢,平衡时溶浸时间增长。
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:

已知298K时, Ksp(CaCO3)=2.80×10―9, Ksp(CaSO4)=4.90×10―5?,求此温度下该反应的平衡常数K?。
参考答案:(1)CaSO4(1分) Mg(OH)2(1分)
(2)氢氧根与镁离子结合,使平衡向右移动,K+变多。(2分)
(3)K2CO3 (2分)?H2SO4 (2分)
(4)①③(2分)
(5)K=1.75×104(3分)
本题解析:(1)根据题目给出的可逆溶解平衡,加Ca(OH)2后,Mg 2+变成Mg(OH)2,硫酸钙是微溶物,因此滤渣成分是Mg(OH)2,CaSO4和未溶杂卤石;(2)根据勒夏特列原理,加入Ca(OH)2后,Mg 2+不断沉淀,硫酸钙也析出,平衡正移,因此浸出K+;(3)为了使生成的硫酸钾最纯,要除去加入的过量的氢氧化钙,而进入杂质阳离子,因此加入碳酸钾,最后硫酸钾除去过量的碳酸钾且调节溶液pH值;(4)由已知曲线图观察可知,升高温度可以提高K+浸出率,缩短浸出时间;(5)由题意知:Ksp(CaCO3)=2.80×10-9=c(Ca2+)・c(CO32-),Ksp(CaSO4)=4.90×10-5=c(Ca2+)・c(SO42-),因此有:Ksp =1.75×104。
点评:本题在化学工艺流程的背景下对化学反应平衡进行考查,题目难度比较大,综合性较强。
本题难度:一般
3、选择题 在密闭容器中,下列可逆反应达到平衡后,升高温度可以使混合气体平均相对分子质量减小的是
A.H2(g)+Br2(g) 2HBr(g)ΔH<0
2HBr(g)ΔH<0
B.N2(g)+3H2(g) 2NH3(g)ΔH<0
2NH3(g)ΔH<0
C.A(s) B(s)+ C(g)ΔH>0
B(s)+ C(g)ΔH>0
D.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
参考答案:B
本题解析: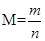 ;升高温度,ABD逆向移动,但只有B的体积增大,即质量不变条件下,物质的量增大,M减小。故B正确。
;升高温度,ABD逆向移动,但只有B的体积增大,即质量不变条件下,物质的量增大,M减小。故B正确。
本题难度:一般
4、选择题 反应2A(g)+B(g)2C(g);△H>0。下列反应条件有利于生成C的是
A.低温、低压
B.低温、高压
C.高温、高压
D.高温、低压
参考答案:C
本题解析:该反应的正反应为气体总体积减小的吸热反应,因此高压、高温有利于C的生成,故选C。
本题难度:一般
5、选择题 下列有关化学反应速率的说法中,正确的是?
A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B.用铁片和稀硫酸反应制取氢气,改用铁片和浓硫酸可以加快产生氢气的速率
C.在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体可加快溶液褪色速率
D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,若升高温度,则吸热反应速率增大,放热反应速率减小
参考答案:C
本题解析:试题分析:氯化钠溶液和铁不反应,但溶液的体积增加,氢离子的浓度降低,反应速率降低,所以选项A不正确;常温下铁在浓硫酸中发生钝化,得不到氢气,B错误;C中硫酸锰起到催化剂的作用,可以加快反应速率,C正确;只要温度升高,反应速率都是增大的,D不正确,答案选C。
考点:考查外界条件对化学反应速率的影响
点评:该题是高考中的常见题型和重要考点,属于中等难度试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生对化学反应速率概念以及外界条件对反应速率影响的熟悉了解程度,旨在考查学生灵活运用基础知识解决实际问题的能力。有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:困难