1、填空题 (15分)氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用。
(1)已知25℃时,几种难溶电解质的溶度积如下表所示:
氢氧化物
| Cu(OH)2
| Fe(OH)3
| Fe(OH)2
| Mg(OH)2
|
Ksp
| 2.2×10-20
| 4.0×10-38
| 8.0×10-16
| 1.8×10-11
|
向Cu2+、Mg2+、Fe3+、Fe2+浓度都为0.01mol・L-1的溶液中缓慢滴加稀氨水,产生沉淀的先后顺序为 (用化学式表示)。
(2)实验室制备氨气的化学方程式为 。
工业上,制备肼(N2H4)的方法之一是用次氯酸钠溶液在碱性条件下与氨气反应。以石墨为电极,将该反应设计成原电池,该电池的负极反应为 。
(3)在3 L密闭容器中,起始投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
温度(K)
| 平衡时NH3的物质的量(mol)
|
T1
| 2.4
|
T2
| 2.0
|
已知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1 T2(填“>”、“<”或“=”)。
②在T2 K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)= ,平衡时N2的转化率α(N2)= 。若再增加氢气浓度,该反应的平衡常数将 (填“增大”、“减小”或“不变”)。
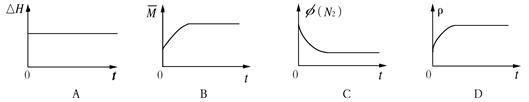
③下列图像分别代表焓变(△H)、混合气体平均相对分子质量(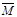 )、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是 。
)、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是 。
参考答案:(1)Fe(OH)3、Cu(OH)2、Fe(OH)2、Mg(OH)2(2分,顺序不正确不得分)
(2)2NH4Cl+Ca(OH)2 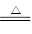 CaCl2+2NH3↑+2H2O(2分,未标加热或气体符号或未配平扣1分)
CaCl2+2NH3↑+2H2O(2分,未标加热或气体符号或未配平扣1分)
2NH3+2OH--2e-=N2H4+2H2O(2分)
(3)①<(2分) ②0.1 mol?L-1?min-1 (2分) 25%(2分)不变(1分) ③BC(2分)
本题解析:(1)溶度积常数越小,越溶液产生沉淀,根据溶度积常数大小可知产生沉淀的先后顺序是Fe(OH)3、Cu(OH)2、Fe(OH)2、Mg(OH)2。
(2)实验室利用熟石灰与氯化铵加热制备氨气,反应的化学方程式为2NH4Cl+Ca(OH)2 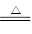 CaCl2+2NH3↑+2H2O;原电池中负极失去电子发生氧化反应,因此氨气在负极通入,失去电子转化为肼,所以该电池的负极反应为2NH3+2OH--2e-=N2H4+2H2O。
CaCl2+2NH3↑+2H2O;原电池中负极失去电子发生氧化反应,因此氨气在负极通入,失去电子转化为肼,所以该电池的负极反应为2NH3+2OH--2e-=N2H4+2H2O。
(3)①已知破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量,这说明该反应是放热反应。根据表中数据可知T1时生成的氨气多,温度低有利于氨气的生成,所以T1<T2。
②平衡时氨气的物质的量是2mol,则根据方程式N2+3H2 2NH3可知消耗氢气的物质的量是3mol,浓度是1mol/L,所以0~10min内H2的平均速率v(H2)=1mol/L÷10min=0.1 mol?L-1?min-1 ;消耗氮气的物质的量是1mol,所以氮气的转化率是
2NH3可知消耗氢气的物质的量是3mol,浓度是1mol/L,所以0~10min内H2的平均速率v(H2)=1mol/L÷10min=0.1 mol?L-1?min-1 ;消耗氮气的物质的量是1mol,所以氮气的转化率是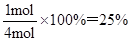 ;平衡常数只与温度有关系,因此若再增加氢气浓度,该反应的平衡常数将不变。
;平衡常数只与温度有关系,因此若再增加氢气浓度,该反应的平衡常数将不变。
③在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A、对于具体的化学方程式反应热是不变,因此反应热不变不能表明该可逆反应达到平衡状态,A错误;B、混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以当平均相对分子质量不再发生变化时,能表明该可逆反应达到平衡状态,B正确;C、当氮气含量不再发生变化时,可以说明反应达到平衡状态,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,即密度始终是不变,D错误,答案选BC。
考点:考查溶度积常数应用、氨气制备、电极反应式书写、化学平衡状态的判断、计算等
本题难度:困难
2、选择题 已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)= 2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
[? ]
A.AgCl>AgI>Ag2CrO4
B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI>AgCl
参考答案:C
本题解析:
本题难度:一般
3、选择题 已知25℃时一些难溶物质的溶度积常数如下:
化学式
| Zn(OH)2
| ZnS
| AgCl
| Ag2S
| MgCO3
| Mg(OH)2
|
溶度积
| 5×10-17
| 2.5×10-22
| 1.8×10-10
| 6.3×10-50
| 6.8×10-6
| 1.8×10-11
|
?
根据上表数据,判断下列化学方程式不正确的是(? )
A.2AgCl+Na2S=2NaCl+Ag2S
B.MgCO3+H2O△,Mg(OH)2+CO2↑
C.ZnS+2H2O=Zn(OH)2+H2S↑
D.Mg(HCO3)2+2Ca(OH)2=Mg(OH)2↓+2CaCO3↓+2H2O
参考答案:C
本题解析:根据溶度积常数可知,溶解度:ZnS<Zn(OH)2,由于发生复分解反应时生成溶解度更小的物质,故C不正确。
本题难度:一般
4、填空题 炼锌厂产生的工业废渣――锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4・7H2O和金属镉(Cd)是一个有益的尝试,其流程如下:
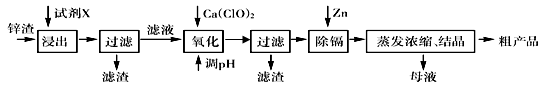
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7。试回答下列问题:
(1)浸出时用到的试剂X为?, 写出溶解过程中加快浸出速率和提高浸出率的两点措施:_______________________________,______________________________。
(2)写出加入Ca(ClO)2反应的离子方程式?。
(3)调节pH过程可以选用?(填“ZnO”或“NaOH”);本流程的pH调节一般调至5,其目的是??。
(4)写出过滤后加入过量的锌粉反应的离子方程式?。
(5)在蒸发浓缩操作时,要采取实验措施是:?。
参考答案:(1)H2SO4溶液?适当升温、充分搅拌、延长溶解时间等(其它答案合理也给分)
(2)2H++ClO―+2Fe2+ =Cl―+2Fe3++H2O(配平错扣1分)
(3)ZnO ,除去Fe3+和Al3+,防止Zn2+沉淀析出
(4)Zn+Cd2+=Zn2++Cd?(5)保持一定的酸度(其它表达合理也给分)
本题解析:(1)本题是制备硫酸锌晶体的的工艺流程,锌渣中含有难溶的二氧化硅杂质,选用酸溶除去二氧化硅,考虑尽量少引入杂质,应选含有硫酸根离子的硫酸溶液进行溶解。若要加快浸出速率和提高浸出率,可以适当升高温度或搅拌溶液或适当延长时间等。
(2)用硫酸浸出的滤液中含有少量Fe3+、Al3+、Zn2+、Cd2+、Fe2+ 等离子,考虑这些离子分别沉淀的pH值,应该把Fe2+ 氧化为Fe3+ 在沉淀除去,所以加入氧化剂Ca(ClO)2 发生的反应方式为:2H++ClO―+2Fe2+ =Cl―+2Fe3++H2O。
(3)由于整个流程制备的是硫酸锌晶体,所以在调节pH时要注意不能引入杂质,所以应该选用ZnO调节,而调节pH值到5左右目的是使容易沉淀的Fe3+、Al3+ 先沉淀除去,防止pH过高把生成的Al(OH)3溶解、把Zn2+ 沉淀。
(4)在上步调节完pH后,溶液中还存在杂质离子Cd2+ ,由于Cd2+ 沉淀的pH值与Zn2+ 沉淀的pH值相近,所以不能用沉淀法除去,所以要加入单质Zn把Cd置换出来,因此发生的离子方程式为:Zn+Cd2+=Zn2++Cd。
(5)硫酸锌在蒸发浓缩时容易发生水解,所以为了减少水解产生杂质,应该保持溶液一定的酸度。
本题难度:困难
5、填空题 (1)对于Ag2S(s) 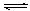 2Ag+(aq)+ S2-(aq),其Ksp=____________。
2Ag+(aq)+ S2-(aq),其Ksp=____________。
(2)下列说法不正确的是__________。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的;
C.对于Al(OH)3(s) 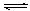 Al(OH)3(aq)
Al(OH)3(aq) 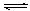 Al3++3OH-,前者为溶解平衡,后者为电离平衡;
Al3++3OH-,前者为溶解平衡,后者为电离平衡;
D.除溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大