1、选择题 4p轨道填充一半的元素,其原子序数是
A.15
B.35
C.51
D.33
2、填空题 (9分)五种短周期元素A、B、C、D、E原子序数逐渐增大。A和B在同一周期,A是同周期元素中半径最大的(不包含稀有气体);B原子的次外层电子数是最外层电子数的4倍;C是同周期简单离子中半径最小的元素;D元素原子的p轨道有3个未成对电子;E原子的K、L层电子数之和比K、M层电子数之和多1个。
(1)写出E元素基态原子的外围电子排布式?
(2)比较第一电离能的大小:B?C(填大于、小于或等于)
(3)分别写出D、E的最高价氧化物对应水化物的化学式?、?,并比较二者酸性(或碱性)的强弱?(填大于、小于或等于)
(4)写出B的最高价氧化物对应水化物与E的最高价氧化物对应水化物反应的离子方程式?
(5)写出C的最高价氧化物对应水化物与A 的最高价氧化物对应水化物反应的化学方程式?
的最高价氧化物对应水化物反应的化学方程式?
3、选择题 据报道,放射性同位素钬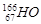 可有效冶疗肝癌,该同位素原子核内的中子数与质子数之差为(?)
可有效冶疗肝癌,该同位素原子核内的中子数与质子数之差为(?)
A.32
B.67
C.99
D.166
4、填空题 (14分)X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
元素
| 相关信息
|
X
| X的基态原子核外3个能级上有电子,且每个能级上的电子数相等
|
Y
| 原子最外层电子数是次外层的三倍
|
Z
| 单质及其化合物的焰色反应为黄色
|
W
| W元素基态原子的M层全充满,N层只有一个电子
|
⑴ X位于元素周期表第?族 。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于?晶体。
。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于?晶体。
⑵ X与Y中电负性较强的是(填元素符号)?;XY2的电子式是?,分子中存在?个σ键。
⑶Z2Y2中含有的化学键类型有?。阴、阳离子的个数比为?。
⑷W的基态原子核外电子排布式是?。
⑸废旧印刷电路板上有W的单质A。用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A。已知:
A(s)+H2SO4(aq) ="=" ASO4(aq) + H2(g) ? ΔH=+64.4kJ・mol-1
2H2O2(l) ="=" 2H2O(l) + O2(g) ?ΔH= -196.4kJ・mol-1
H2(g)+ O2(g) ="=" H2O(l) ?ΔH= -285.8kJ・mol-1
O2(g) ="=" H2O(l) ?ΔH= -285.8kJ・mol-1
请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):
? 。
5、填空题 短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;下图是元素周期表的一部分,编号为③的元素最外层与最内层电子数等
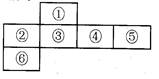
(1)编号为⑤的元素的符号为?,其在周期表中位于?。
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:?。
(3)己知AlCl3的熔点为190 ℃(2.5×105Pa),沸点为182.7℃,
试推测:
①BeCl2是?化合物(填“离子”或“共价”),
②Be(OH)2的碱性比LiOH ?。
(4)根据Mg在空气中的燃烧情况, Li在空气中燃烧生成的产物为? __(用化学式表示)。