1、选择题 进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。下图中能正确表示实验结果的是(?)
参考答案:C
本题解析:固体反应物的接触面积越大,反应速率越快,所以B中反应速率快。10g碳酸钙需要0.2mol盐酸,5g碳酸钙需要0.1mol盐酸,所以在反应中A中碳酸钙过量,最终生成的CO2是相等的,因此答案选C。
本题难度:一般
2、计算题 在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定条件下发生如下反应:2H2(g) +? CO(g) CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
(1)以H2的浓度减少量来表示的反应速率。
(2)达到平衡时CO的转化率。
参考答案:(1)0.8mol/(L・min)?(2)50%
本题解析:考查化学反应速率和化学平衡的有关计算,一般采用三段式。
平衡时甲醇的物质的量是2mol/L×0.5L=1mol,则
2H2(g) +? CO(g) CH3OH(g)
CH3OH(g)
起始量(mol)? 5? 2? 0
转化量(mol)? 2? 1? 1
平衡量(mol)? 3? 1? 1
所以(1)以H2的浓度减少量来表示的反应速率是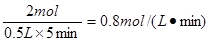
(2)达到平衡时CO的转化率是1÷2×100%=50%
本题难度:简单
3、选择题 某学习小组为了探究?BrO3-+5Br-+6H+=3Br2+3H2O?反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:
实验编号
相关数据 | ① | ② | ③ | ④ | ⑤
c(H+)/mol?L-1
0.008
0.008
0.004
0.008
0.004
c(BrO3-)/mol?L-1
0.001
0.001
0.001
0.002
0.002
c(Br-)/mol?L-1
0.10
0.20
0.20
0.10
0.40
v/mol?L-1?s-1
2.4×10-8
4.8×10-8
1.2×10-8
4.8×10-8
v1
|
下列结论不正确的是( )
A.若温度升高到40℃,则反应速率增大
B.实验②、④,探究的是c(BrO3-)对反应速率的影响
C.若该反应速率方程为v=k?ca(BrO3-)cb(Br-)cc(H+)(k为常数),则c=2
D.实验⑤中,v1=4.8×10-8mol?L-1?s-1
参考答案:A、由于温度升高,反应速率增大,故A正确;
B、实验②、④中,c(Br-)也不相同,故B错误;
C、②、③中,氢离子浓度增大1倍,速率增大到原来的4倍,故c=2,故C正确;
D、③、⑤中,c(Br-)和c(BrO3-)浓度关系,⑤中的二者浓度都比③中的增大一倍,速率增大4倍,v1=4.8×10-8mol?L-1?s-1,故D正确;
故选B.
本题解析:
本题难度:简单
4、选择题 CO(g)+H2O(g) H2(g)+CO2(g)ΔH
H2(g)+CO2(g)ΔH
参考答案:
本题解析:
本题难度:一般
5、选择题 四氯化硅还原法是当前制备较高纯度硅的一种方法,有关反应的化学方程式为:
?
SiCl4(g)+2H2(g) ="===Si" (s)+4HCl(g)。下列说法合理的是?(?)
A.光导纤维的主要成分是硅单质
B.减小压强有利于加快化学反应速率
C.高温下,氢气的还原性强于硅
D.混入少量空气对上述反应无影响
参考答案:C
本题解析:略
本题难度:一般