1、选择题 已知部分化合物的溶度积常数见下表:
化学式
| Ksp
| 化学式
| Ksp
|
AgBr
| 5.0×10-13
| Ag2CO3
| 8.1×10-12
|
Ag3PO4
| 1.4×10-16
| CaCO3
| 2.8×10-9
|
AgOH
| 2.0×10-8
| Ca3(PO4)2
| 2.0×10-29
|
?
现有某种KNO3溶液,其中混有少量KBr和Ca(H2PO4)2杂质,可供选择的试剂有:①AgNO3,②K2CO3,③KOH,④HNO3。若规定不得重复使用试剂,且最后溶液中只允许含有K+、NO3-和少量H+、OH-,则加入试剂顺序正确的是
A.③①②④
B.①③②④
C.②①③④
D.①②③④
参考答案:A
本题解析:略
本题难度:简单
2、填空题 重金属离子(Cu2+、Hg2+、Cd2+、Pb2+等)是常见的有毒污染物,水体、土壤及生物一旦受到重金属离子的污染就很难去除,重金属污染给生态环境和人类自身造成严重危害.某公司以含重金属的废水为原水,处理废水工艺流程如图1所示:

已知下列物质的Ksp:
| Cu(OH)2 | CuS | FeS | PbS | HgS | CdS
2.2×10-20
8.5×10-45
6.3×10-18
3.4×10-28
4×10-53
8×10-29
|
请回答下列问题:
(1)OH-与S2-相比,除去废水中的Cu2+效果较好的是______.
(2)图2为某些重金属离子在不同温度与pH下的平衡浓度:
从图中分析,除去废水中的重金属离子的最佳温度为______,上述流程中NaOH的作用是调节溶液的PH为______.
参考答案:(1)由表中数据可知Ksp(CuS)<<Ksp[Cu(OH)2],所以CuS在水中溶解度比Cu(OH)2小,所以OH-与S2-相比,除去废水中的Cu2+效果较好的是S2-;
故答案为:S2-;
(2)由图中数据可知在60℃左右时重金属离子的浓度最低,所以除去废水中的重金属离子的最佳温度为:60℃;由图中数据可知PH在8.8~9.0时重金属离子浓度最低,所以NaOH的作用是调节溶液的PH为8.8~9.0;
故答案为:60℃;调节溶液的PH为8.8~9.0.
本题解析:
本题难度:一般
3、选择题 下列有关说法正确的是( )
A.赤潮、酸雨、臭氧层空洞、潮汐等都与环境污染有关
B.Ksp反映了物质在水中的溶解能力,可直接根据Ksp的数值大小比较电解质在水中的溶解能力大小
C.汽油、柴油和植物油都是碳氢化合物
D.“神舟六号”飞船返回舱的表层采用高温时自动烧蚀的耐高温、抗氧化的新型无机非金属材料带走热量从而保证内部温度不致过高
参考答案:A.赤潮、酸雨、臭氧层空洞都与环境污染有关,而潮汐为自然现象,与环境污染无关,故A错误;
B.同类型电解质(阴阳离子个数比相等)Ksp越大溶解性越大,说明难溶物在水中的溶解能力越强.对阴阳离子个数比不同的难溶物,则必须通过计算判断,如AgCl与Fe(OH)3,二者的阴阳离子个数比不同,不能简单地根据Ksp进行比较,故B错误;
C.植物油为烃的含氧衍生物,不属于碳氢化合物,即不属于烃类物质,故C错误;
D.自动烧蚀的耐高温、抗氧化的新型无机非金属材料在飞船返回舱的表层可在高温下“升华”和“蒸发”从而带走了舱的热量,从而保证内部温度不致过高,故D正确.
故选D.
本题解析:
本题难度:一般
4、选择题 常温下,2.0×10-3mol?L-1氢氟酸的水溶液中,调节溶液pH(忽略溶液体积变化)得到的[HF]、[F-]与溶液pH的变化关系如下图.下列叙述不正确的是( )
(提示:Ka(CH3COOH)=1.8×10-5mol?L-1,Ksp(CaF2)=1.5×10-10mol3?L-3)
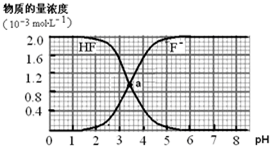
A.两条曲线交点a对应溶液的[F-]=[HF]
B.加入NaOH溶液至pH=7,溶液中[F-]=[Na+]
C.常温下HF的电离常数Ka(HF)>Ka(CH3COOH)
D.pH=4时,加入CaCl2固体使[Ca2+]=2.0×10-3mol?L-1,无CaF2沉淀析出
参考答案:A、纵轴是微粒浓度,横轴是溶液PH,两条曲线交点a对应溶液的[F-]=[HF],故A正确;
B、加入NaOH溶液反应HF+NaOH=NaF+H2O;溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(F-),至pH=7,c(H+)=c(OH-),溶液中[F-]=[Na+],故B正确;
C、Ka=c(H+)c(F-)c(HF);当c(F-)=C(HF)时,Ka=c(H+)=10-3.5=3.5×10-4mol?L-1>Ka(CH3COOH)=1.8×10-5mol?L-1,常温下HF的电离常数Ka(HF)>Ka(CH3COOH),故C正确;
D、分析图象当PH=4.0,溶液中的F-离子浓度1.6×10-3mol;加入CaCl2固体使c(Ca2+)=2.0×10-3mol?L-1,c(Ca2+)×c2(F-)=2.0×10-3mol?L-1×(1.6×10-3)2=5.1×10-10>Ksp(CaF2),有沉淀生成,故D错误;
故选D.
本题解析:
本题难度:简单
5、选择题 下列有关沉淀溶解平衡的说法正确的是( )
A.KSP(AB2)小于KSP(CD),则物质AB2的溶解度一定小于物质CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
参考答案:A、因比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,故A错误;
B、因难溶盐电解质的Ksp与温度有关,不受其他因素的影响,所以加入蒸馏水,氯化银的KSP不变,故B错误;
C、因氯化银的溶度积大于碘化银的溶度积,所以氯化银沉淀可转化为碘化银沉淀,故C正确;
D、碳酸根离子与酸反应生成二氧化碳和水,生成物的浓度减小,碳酸钙的沉淀溶解平衡正向移动,故D错误;
故选:C.
本题解析:
本题难度:简单