1��ѡ���� �����۷����Ȼ�ͭ���Ȼ����Ļ����Һ�У���ַ�Ӧ������ȫ���ܽ⡣�ɴ˿��ж�����˵����ȷ����
A������ͭ��������Һ����Cu2+��Fe2+��Fe3+����
B������ͭ��������Һ����Cu2+��Fe2+���ӣ�Ҳ������Fe3+����
C������ͭ��������Һ����Fe2+���ӣ�û��Cu2+��Fe3+����
D������ͭ��������Һ����Fe2+���ӣ�������Cu2+���ӣ�Ҳ������Fe3+����
�ο��𰸣�B
�������������������Fe3+��Cu2+�������ӷ�Ӧ����Fe��2Fe3��=3Fe2���� Fe��Cu2��=Cu��Fe2��
����ͭ������˵����Ӧ�ٿ���ȫ�����лֽ��У���Ӧ��û�з�������A����ȷ��B��ȷ
����ͭ��������Ӧ����ȫ�����У���Ӧ�ڿ��ܲ��ֽ��У�Ҳ����ǡ����ȫ��Ӧ����Һ����Fe2+���ӣ�������Cu2+���ӣ������Բ�������Fe3+���ӣ��ų�CD
��ΪB
�����Ѷȣ�һ��
2������� �ס�����ͬѧ����ͼ��ʾװ�ý���ʵ�飬̽������������Ӧ�IJ��
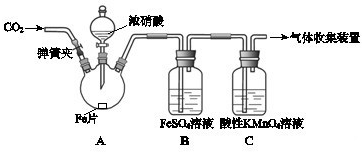
�����أ�I����Ũ����ͻ��ý�����Ӧ�����У���������Ũ�ȵĽ��ͣ������ɵIJ�����+4��+2��-3�۵ȵ��Ļ����
II��FeSO4+NO?Fe��NO��SO4����ɫ����H��0��
III��NO2��NO���ܱ�KMnO4�������գ�
��ʵ������������¼���£�
| ʵ����� | ʵ������
���ɼУ�ͨ��һ��ʱ��CO2���رյ��ɼУ�
��Һ©����������Ũ���Ỻ��������ƿ�У��رջ�����
����������
������ƿ����Ӧ��ʼ��ֹͣ���ȣ�
��A���к���ɫ���������һ��ʱ���������ɫ��dz��?B����Һ����ɫ��?C����Һ��ɫ��dz��
�ڷ�Ӧֹͣ��A������ʣ�࣮
|
��ش��������⣺
��1������Ũ�������ǰû�����������ԭ����______��
��2�������Ƿ�����-3�۵��Ļ����Ӧ���е�ʵ�������______��
��3����ȡ����B����Һ�����ȣ�ʵ��������______�����û�ѧƽ��ԭ������ԭ��______�������ݸ�����ó��Ľ�����A����NO���ɣ�
��4������Ϊ�ó�A����NO���ɵ�֤�ݲ��㣮Ϊ��ȡ�����֤�ݣ����Բ��ø�װ�úͲ������ж���ʵ�飬�������ĸı���______��֤����NO���ɵ�ʵ��������______��
��5��֤��A��Һ���Ƿ���Fe2+��Fe3+��ѡ���ҩƷ�ǣ�����ţ�______��
a������?b����ˮ?c����軯����Һ?d�����軯����Һ��
�ο��𰸣���1������ʱ������Ũ���ᷴӦ����һ�����ܵ������ﱡĤ����ֹ������Ũ�����һ����Ӧ���������ۻ��������Ե���Ũ�������ǰû����������
�ʴ�Ϊ������ʱ������Ũ�����γ���������Ĥ����ֹ��Ӧ��һ��������
��2������-3�۵��Ļ������ǰ�����������������ˮ���ɰ�ˮ����ˮ��������笠����ӣ�����笠����ӵķ����ǣ�ȡ������Ӧ��A����Һ���Թ��У������м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�ӽ��Թܿڣ�����ֽ��������A������NH4+���ʴ�Ϊ��ȡ������Ӧ��A����Һ���Թ��У������м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�ӽ��Թܿڣ�����ֽ��������A������NH4+��
��3��ȡ����B����Һ�����ȣ���ɫ���ڱ�dz������ɫ�����ݳ����Ҹ������ڿ����б�Ϊ����ɫ��ӦΪ���淴ӦFeSO4+NO?Fe��NO��SO4����ɫ���Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�������Fe��NO��SO4����ɫ�����ͣ�������Һ��ɫ��dz���ʴ�Ϊ����ɫ��Һ��dz�����̣�����ɫ�����ݳ������ڿ����б�Ϊ����ɫ��FeSO4+NO?Fe��NO��SO4����ɫ����H��0?����Ӧ���ȣ����Ⱥ�ƽ�����淴Ӧ�����ƶ���
��4������������ˮ��Ӧ���ɵ�һ��������ʹ����������Һ�����ɫ�����Բ���֤������Ũ���ᷴӦ������NO���ɣ�Ϊ�ų����ɵ�NO���ţ���Ũ���ỻ��ϡ���ᣬϡ�����ͭ��Ӧ������ɫ��һ��������û�ж����������ɣ���A����������ɫ�ģ���B����Һ��Ϊ��ɫ����˵�����ɵ�һ������������������Ӧ������ɫ���Ӷ�˵��A����ɫ������һ��������
�ʴ�Ϊ��Ũ���ỻ��ϡ���A��û�к���ɫ�������ɣ�B����Һ��Ϊ��ɫ��
��5���������ӵ�������Ӧ�ǣ��������Ӻ����軯����Һ��Ӧ������ɫ�����������ӵ�������Ӧ�ǣ������Ӻ���ɫ�����軯����Һ��ӦѪ��ɫ��Һ����ѡcd��
���������
�����Ѷȣ�һ��
3��ʵ���� ij�Ȼ��������Ȼ����Ļ�����Ҫ�ⶨ������Ԫ�ص�������������������ʵ�飺

��ͬѧ�����������̽���ʵ�飬�ش��������⣺
��1�����������õ��IJ����������ձ����������⣬��������?��?�����������ƣ�
��2����д��������ˮ���������ӷ�Ӧ����ʽ?��
��3�������������������м��������غ���ȴ�����£�����ʣ���������������������㡣
ʵ���м��������ص�Ŀ����?��
��4��������������W1g����������Ⱥ������������W2g������Ʒ����Ԫ�ص�����������?��
����ͬѧ����������Բ������·������ⶨ��
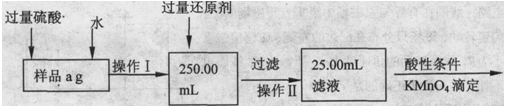
��1���ܽ���Ʒ���������ᣬ�����ӷ���ʽָ������������ԭ����?��
��2����Ҫ��ʵ��֤��������������Һ�в�����Fe3+������ɿ��Ļ�ѧ������?��
��3�����ζ��õ�c mol��L KMn04��Һb mL������Ʒ����Ԫ�ص�����������?��
�ο��𰸣���1��250mL����ƿ��1�֣�����ͷ�ιܣ�1�֣�
��2��2Fe2+��Br2��2Fe3+��2Br����2�֣�
��3��ʹFe��OH��3�ֽ���ȫ��2�֣�
��4��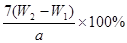 ?��2�֣�
?��2�֣�
��1��2MnO4- +16H+ +10Cl- =2Mn2+ +5Cl2 +8H2O��2�֣�
��2��ȡ������Һ���Թ��У��μ�1~2��KSCN��Һ����Һ����죨2�֣�
��3��2��8bc/a��2�֣�
�����������1������һ�����ʵ���Ũ�ȵ���Һ����Ҫ�������У���ͷ�ιܡ��ձ�����������һ����������ƿ�����Ի�ȱ��250mL����ƿ����ͷ�ιܡ�
��2��������ˮ���嵥�������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2+Br2=2Fe3++2Br-��
��3�����������أ�˵��Fe��OH��3�ֽ���ȫ��
��4������������W1g����������Ⱥ������������W2g�������ɵ�����������Ϊ��W2-W1��g��25ml��Һ����Ԫ�ص�����=112/160��W2-W1��g��250ml�к�����Ԫ������10��112/160��W2-W1��g��������Ԫ����������=��100%=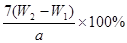
��1��MnO4?�ܰ�Cl?����ΪCl2�����ӷ���ʽΪ��2MnO4- +16H+ +10Cl- =2Mn2+ +5Cl2 +8H2O
��2�����鲻����Fe3+��Ӧʹ��KSCN��Һ�����Է����ǣ�ȡ������Һ���Թ��У��μ�1~2��KSCN��Һ����Һ����졣
��3������MnO4?����Fe2+�����ӷ���ʽ��5Fe2++MnO4-+16H+=Mn2++5Fe3++8H2O��25.00mL��Һ��? n��Fe2+��=5n��MnO4?��=5bc��10-3mol����250ml��Һ�к���Ԫ�����ʵ���Ϊ5bc��10-2mol��������Ʒ����Ԫ�ص���������=5bc��10-2mol��56g/mol��ag=2��8bc/a ��
�����Ѷȣ�һ��
4������� 1 g CuO��ľ̿�۵Ļ����ڸ��������������¼���һ��ʱ�䲢��ȴ��������Ϊ x g��
����Ӧ��ֻ����CO2��
��1��ʵ������?g ?CuO����ԭ��?��2��x��ȡֵ��Χ��?��
�ο��𰸣���1��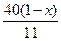 ?����2��
?����2��
�����������
�����Ѷȣ���
5��ѡ���� a g�����뺬��H2SO4��CuSO4��Һ��ȫ��Ӧ�õ�a gͭ������뷴Ӧ��CuSO4��
 H2SO4�����ʵ���֮��Ϊ?��?��
H2SO4�����ʵ���֮��Ϊ?��?��

A��1 ��7
B��7 ��1
C��7 ��8
D��8 ��7
�ο��𰸣�B
��������� �����������֪����������ȫ��Ӧ�ҷ�Ӧǰ�������������䣬�����μӷ�Ӧ��CuSO4��H2SO4�����ʵ����ֱ�Ϊx��y����
�����������֪����������ȫ��Ӧ�ҷ�Ӧǰ�������������䣬�����μӷ�Ӧ��CuSO4��H2SO4�����ʵ����ֱ�Ϊx��y����
 Fe ��CuSO4?="?" FeSO4��Cu?��m
Fe ��CuSO4?="?" FeSO4��Cu?��m
 ? 1mol? 56g
? 1mol? 56g
 ? x? 56 x g��mol��1
? x? 56 x g��mol��1
 Fe ��H2SO4? ="?" FeSO4��H2��?��m
Fe ��H2SO4? ="?" FeSO4��H2��?��m
 1mol? 8g
1mol? 8g
 ?y? 8 y g��mol��1
?y? 8 y g��mol��1
 ��Ӧǰ����������û�з����仯����˵�һ����Ӧ�����ļ�С���ڵڶ�����Ӧ���������ӣ���56x g��mol��1="8" y g��mol��1������
��Ӧǰ����������û�з����仯����˵�һ����Ӧ�����ļ�С���ڵڶ�����Ӧ���������ӣ���56x g��mol��1="8" y g��mol��1������ ��
��
�����Ѷȣ�һ��