| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《化学反应速率》试题预测(2017年最新版)(八)
参考答案: 本题解析:略 本题难度:一般 4、选择题 一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2?(g)△H>0,以下说法中正确的是( )
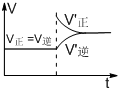
C.增大压强后,V正、V逆如图所示 D.利用该反应原理可以在铁表面附上一层保护层,减少铁的腐蚀 |
参考答案:A.反应吸热,升高温度平衡向正反应方向移动,H2O(g)的转化率增大,故A正确;
B.反应的化学平衡常数的表达式为k=c(H2)4c(H2O)4,故B错误;
C.增大压强,正逆反应速率都增大,由于反应前后气体的化学计量数之和相等,则平衡不移动,故C错误;
D.利用该反应原理可以在铁表面生成一层致密的Fe3O4,起到保护层的作用,故D正确.
故选AD.
本题解析:
本题难度:简单
5、选择题 2SO2(g)+O2(g)  ?2SO3(g) 是制备硫酸的重要反应。下列叙述正确的是
?2SO3(g) 是制备硫酸的重要反应。下列叙述正确的是
[? ]
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是C1、C2,则时间间隔t1-t2内,SO3(g)生成的平均速率为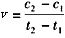
参考答案:D
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《物质的分类.. | |