1、实验题 测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与I-反应成I3-,并在溶液中建立如下
平衡:I2 +I-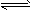 I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I、某同学为测定上述平衡体系中c(I2),采用如下方法:取V1 mL平衡混合溶液,用cmol・L-1的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗V2 mL的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。
(1)上述滴定时,可采用_________做指示剂,滴定终点的现象是________。
(2)下列对该同学设计方案的分析,正确的是__________(填字母)。
A.方案可行。能准确测定溶液中的c(I2)
B.不可行。因为I-能与Na2S2O3发生反应
C.不可行。只能测得溶液中c(I2)与c(I3-)之和
Ⅱ、化学兴趣小组对上述方案进行改进,拟采用下述方法来测定该反应的平衡常数(室温条件下进行,溶液体积变化忽略不计)
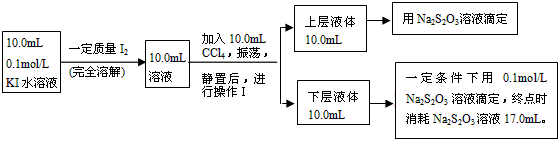
已知:①I-和I3-不溶于CCl4;②一定温度下碘单质在四氯化碳和水混合液体中,碘单质的浓度比值
即 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
(3)操作Ⅰ使用的玻璃仪器中,除烧杯、玻璃棒外,还需要的仪器是_________________(填名称)。试指出该操作中应注意的事项为_______________________。(任写一条)
(4)下层液体中碘单质的物质的量浓度是__________。
(5)实验测得上层溶液中c(I3-)=0.049 mol・L-1,结合上述有关数据,计算室温条件下反应
I2+I- I3-的平衡常数K=__________(用具体数据列出计算式即可)。
I3-的平衡常数K=__________(用具体数据列出计算式即可)。
2、选择题 下列实验目的可以达到的是
A.电解熔融氯化镁制取金属镁
B.醋酸钠结晶水合物与碱石灰共热制取甲烷。
C.浓硫酸与溴化钠共热制取溴化氢
D.饱和碳酸钠溶液除去二氧化碳中的氯化氢
3、选择题 下列说法正确的是( )
A.用澄清石灰水可区别Na2CO3和NaHCO3粉末
B.只能用加试 剂的方法区别(NH4)2SO4和Fe2(SO4)3溶液
C.用氯化钡溶液可区别SO42-和CO32-离子
D.用丁达尔效应可区别Fe(OH)3胶体和FeCl3溶液
4、实验题 (1)用简单的实验证明在氨水中存在NH3・H2O NH4++OH-的电离平衡(要求写出简单操作、现象及实验能说明的问题)。 ______________________________________________________。
NH4++OH-的电离平衡(要求写出简单操作、现象及实验能说明的问题)。 ______________________________________________________。
(2)老师给某学生提供下列药品和必要的实验仪器,要求学生设计实验证明醋酸是弱酸。药品为冰醋酸、蒸馏水和pH试纸。此同学思考后认为:
①设计的理论依据是_______________________________;
②实验的简要步骤是_______________________________;
③需记录的现象和数据是___________________________;
④推断与分析:由于_________________,说明________________,所以醋酸是弱酸。
5、选择题 以下是配制250mL0.2mol・L-1氯化钠溶液的步骤:
①溶解?②洗涤?③移液?④计算?⑤定容?⑥称量?⑦盖好瓶塞,反复上下颠倒,摇匀。请你选出该溶液配制的操作先后顺序是(?)
A.②③⑤①⑥⑦④
B.④⑥①③②⑤⑦
C.④②⑤⑥①③⑦
D.②⑥⑦④③⑤①