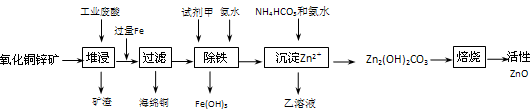
1������� ��14�֣���ij����С����Ƴ����ù�ҵ���ᣨ10%H2SO4�����ѽ�ij����������ͭп����ȡ����ZnO�ķ�����ʵ�ַ����ۺ����ã���������ͼ��ʾ��
��֪��298Kʱ�����ӿ�ʼ��������ȫ����ʱ��pH���±���ʾ��
����
| ��ʼ����ʱ��pH
| ��ȫ����ʱ��pH
|
Fe2��
| 6��34
| 9��7
|
Fe3��
| 1��48
| 3��2
|
Zn2��
| 6��2
| 8��0
|
��ش��������⣺
��1������ͭп���к���������CuS��ZnS����H2SO4��������ZnS�����ܽ��CuS
���ܣ�����������ͬ�¶��£�Ksp��CuS��??Ksp��ZnS����ѡ�������������������
��2������Ϊ�ڳ���������ѡ�����������е�?������ţ���Ϊ�Լ����DZȽϺ��ʵġ�
A��KMnO4? B��O2? C��H2O2? D��Cl2
��3�����������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������?��Χ֮�䡣
��4����д���Ӽ����ʺ��백ˮ���Ƶ�����Һ��pH������Fe��OH��3��Ӧ�����ӷ�
��ʽ?��
��5��298Kʱ������������Һ�е�c��Fe3������ __??mol/L���¡�
[Fe��OH��3��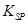 = 2��70��10-39]
= 2��70��10-39]
��6���ҵ���Һ��ֱ���������ʣ����ҵĻ�ѧʽ��?��
��7����д��������Zn2+�������з�����Ӧ�Ļ�ѧ����ʽ?��
�ο��𰸣���14�֣�
��1����?��2�֣�
��2��B C?��2�֣�
��3��3��2~6��2?��2�֣�
��4��Fe3++3NH3��H2O ="==" Fe��OH��3��+3 NH4+ ?��2�֣�
��5��2��7��10-21?��2�֣�
��6����NH4��2SO4?��2�֣�
��7��2ZnSO4 +NH4HCO3 +3 NH3��H2O="=" Zn2��OH��2CO3 ��+2��NH4��2 SO4 + H2O ��2�֣�
�����������1����H2SO4��������ZnS�����ܽ��CuS���ܣ���ȻKsp��CuS����Ksp��ZnS����
��2�����ӵ�ͬʱ���������µ��Ӽ�������A��D����ѡ����H2O2��O2�������£�Fe2+������ΪFe3+���ӡ�
��3������298Kʱ�����ӿ�ʼ��������ȫ����ʱ��pH������֪��Ҫ��Fe3+���ӳ�ֳ�����ȫ��������ʹZn2+������pHӦ������3��2~6��2?��Χ֮�䣻
��4��NH3��H2O���������д���ӷ���ʽʱ���ܲ�����ӵ���ʽ��
��5��Zn2+������pHӦ������8��0���ϣ����ԣ�����������Һ�е�c��Fe3������2��7��10-21?
��6���ҵ���Һ��ֱ������������Ҫ�Ǻ��У�NH4��2SO4��
��7��2ZnSO4 +NH4HCO3 +3 NH3��H2O="=" Zn2��OH��2CO3 ��+2��NH4��2 SO4 + H2O
�����Ѷȣ���
2������� ��ѧ��ȤС��Ϊ̽��ij����ʯ����Ҫ�ɷ�ΪFe203��Si02�������ʣ���������ʵ�飺
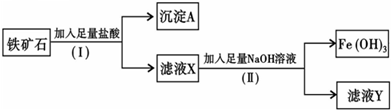
��1�����裨I���з�����Һ�ͳ����IJ���������______��
��2������A��һ������______������������______������ԡ����ԡ��������
��3������ҺY�м���KSCN��Һ����Һ��______�����ɫ����ɫ������
��4��д�����裨��������Fe��OH��3�����ӷ���ʽ______��
�ο��𰸣���1������ʯ����Ҫ�ɷ�ΪFe203��Si02��������������������������ᷴӦ�����Ȼ�����ˮ����������Ϊ�������Ҳ������ᷴӦ������ͨ�����˵ķ������룬
�ʴ�Ϊ�����ˣ�
��2���������費�����ᷴӦ�����Թ��˺�õ��ij���AΪSiO2�����������ܹ���ǿ����Һ��Ӧ�����κ�ˮ�����Զ��������������������
�ʴ�Ϊ��SiO2�����������
��3����Һ�к��������ӣ��������ܹ�����������ӷ�Ӧ���ɺ�ɫ�����軯����
�ʴ�Ϊ����ɫ��
��4�������Ϊ������������������Һ��Ӧ��������������������Ӧ�����ӷ���ʽΪ��Fe3++3OH-�TFe��OH��3����
�ʴ�Ϊ��Fe3++3OH-�TFe��OH��3����
���������
�����Ѷȣ�һ��
3��ѡ���� ��Fe , Cu�Ļ�����м���һ������ϡ���Ტ�ȣ���ַ�Ӧ��ʣ�����a�ˡ��������м���һ������ϡ���Ტ���ȣ������ʣ�����b�ˡ���[
A��aһ������b
B��aһ������b
C��a������b
D��a���ܵ���b
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
4��ѡ���� ��������Һ�зֱ������������һ����ٰ�����ȡ������ʹ�����������ӵ���Һ�ǣ�������
A���Ȼ�þ��Һ
B������������Һ
C������
D������ͭ��Һ
�ο��𰸣�A�������Ȼ�þ��Һ����Ӧ���������䣬��A����
B����������������Һ����Ӧ���������䣬��B����
C���������ᷴӦ�����Ȼ�����������������������С����C����
D�����û���ͭ��ͭ�����ԭ�������������������������ӣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
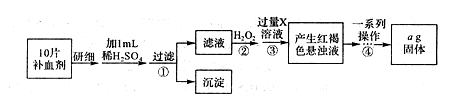
5��ʵ���� ��14�֣�FeSO4��7H2O�㷺����ҽҩ��ҵ����������FeSO4��7H2O��ʵ�����Ʊ�����ͼ�������������������գ�

(1)��м��ϡ���ᷴӦǰ��Ӧ��10% Na2CO3��Һ���ݼ����ӣ�����Ŀ����_____�����ݺ���____����������������벢ϴ����м��
(2)����aΪ_______________��
(3)���õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ��ٳ�ȥ������渽�ŵ���������ʣ�
��____________________��
(4) FeSO4��7H2O��ijЩ��Ѫ������Ҫ�ɷ֣�ʵ����Ҫ�ⶨij��Ѫ������Ԫ�صĺ�����
I������һ������KMn04��Һ����������ԭ�ζ���������100mL 1.00 �� 10 - 2 mol��L-1��KMnO4��Һʱ�����õ���������ƽ��ҩ�ס��ձ���������������___________�����������ƣ��������ƹ����У�����˵����ȷ����____________���������ĸ����
A��KMnO4����ˮ�����ȣ�����ֱ��������ƿ���ܽ�
B������ƿϴ�Ӻ�����T��ֱ������ʵ��
C�����ݺ�ҡ�ȣ���Һ����ڿ̶��ߣ��ټ�ˮ����Һ����͵���̶�����ƽ
D���������ʱ��ˮ�����̶��߱���ع����