1、选择题 若向盛有氯化铁溶液的烧杯中同时加入铁和铜的混合粉末,反应结束后,下列不可能出现的结果是
A.铁、铜都有剩余,溶液中只有Fe2+
B.铁、铜都不剩余,溶液中可能有Fe3+、一定有Fe2+和Cu2+
C.铁有剩余、铜没剩余,溶液中只有Fe2+、Cu2+
D.铁没剩余、铜有剩余,溶液中一定没有Fe3+
参考答案:C
本题解析:略
本题难度:简单
2、填空题 (12分)某校化学研究性学习小组在学习了金属的知识后,探究Cu的常见 化合物的性质。过程如下:
化合物的性质。过程如下:
【提出问题】
①在周期表中,Cu、Al位置接近。Cu不如Al活泼,Al(O H)3具有两性,Cu(OH)2也具有两性吗?
H)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?
③Cu0有氧化性,能被H2、CO等还原,也能被NH3还原吗?
【实验方案】
(1)解决问题①需用到的药品有CuSO4溶液、?、?(填试剂名称),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98 g Cu(OH)2固体,加热至80―100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。冷却后称量,A的质量为72 g,则A的化学式为?。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):
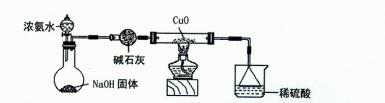
实验中观察到Cu0变为红色物质。查资料可知,同时生成一种无污染的气体。
【实验结论】
(1)Cu(OH)2具有两性。证明Cu(OH)2具有两性的实验现象是?。
(2)根据实验方案(2),得出的+1价Cu相+2价Cu稳定性大小的结论是:在高温时?。在酸性溶液中?。
(3)CuO能够被NH3还原。
【问题讨论】
有同学认为NH3与CuO反应后生成的红色物质是Cu,也有同学认为NH3与CuO反应后生成的红色物质是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应后生成的红色物质中是否含有A?
参考答案:

本题解析:略
本题难度:一般
3、选择题 强酸X的转化关系如图: 图中单质可能为(?)
图中单质可能为(?)
A.C
B.Fe
C.Al
D.Cu
参考答案:D
本题解析:A.单质C在常温下与酸不能发生反应。错误。B.Fe在常温下遇浓硫酸、浓硝酸会发生钝化,不能继续反应。也不符合题意。错误。C.在常温下Al与浓硫酸或浓硝酸发生钝化,产生Al2O3.Al2O3在常温下与水不能反应。错误。D.Cu与浓硝酸反应反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。产生的NO2在水中溶解:3NO2+ H2O = 2HNO3+ NO。得到硝酸。正确。
本题难度:一般
4、选择题 有铁的氧化物样品,用140ml0.5mol/L的盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下氯气56ml,使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是(?)
A.Fe2O3
B.Fe3O4
C.Fe5O7
D.Fe4O5
参考答案:C
本题解析:n(HCl)="0.14L×0.5mol/L=0.07" mol,n(Cl2)="0.0025" mol,由于发生反应:2Fe2++Cl2=2Fe3++2Cl―,(
n(Fe2+),=0.5n(Cl2)="0.005" mol,最后溶液为FeCl3溶液,根据原子守恒可知;3n(Fe2++Fe3+)= n(Fe3+)最后=n(Cl-总)= n(HCl)+2n(Cl2)=" 0.07" mol+0.005 mol ="0.075" mol,所以n(Fe2++Fe3+)="0.025" mol,n(Fe3+)="0.02" mol,n(Fe2+):、n(Fe3+)的比为1:4。然后将选项中的各个复杂的氧化物变形为aFeO .bFe2O3形式。A无Fe2+离子,错误。B化学式变形为FeO .Fe2O3的化合物,二者的物质的量的比为1:2,错误。C.化学式变形为FeO. 2Fe2O3的化合物,二者的物质的量的比为1:4,正确。D 为2 FeO .Fe2O3的化合物,二者的物质的量的比为1:1,错误。
本题难度:一般
5、选择题 对实验Ⅰ~Ⅳ的实验现象判断正确的是( )
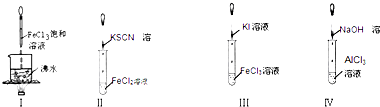
A.实验Ⅰ:产生红褐色沉淀
B.实验Ⅱ:溶液变红色
C.实验Ⅲ:试管中溶液变浅黄色
D.实验Ⅳ:试管中先出现白色沉淀,后溶解
参考答案:D
本题解析:
本题难度:简单