|
�߿���ѧ���⡶������Ƶ����̣�2017�����°棩(��)
2018-03-17 08:17:56
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1�������� (8��)��6.0 g�����ۼ���200 mL Fe2(SO4)3��CuSO4�Ļ��Һ�У���ַ�Ӧ�õ�200 mL ?0.50 mol��L-1 FeSO4��Һ��5.2 g�����������㣺
(1)��Ӧ������ͭ�������Ƕ��٣�
(2)��������ǰFe2(SO4)3��Һ�����ʵ���Ũ�ȡ�
�ο��𰸣�2.56 g? 0.1 mol��L-1
�����������Fe2(SO4)3Ũ��Ϊx mol��L-1������CuΪy mol����Ϊ�õ�200��10-3��0.50="0.1" mol FeSO4������6 g Fe������Feʣ�࣬���У�6-(0.2x+y)��56+y��64="5.2?" ��
y+0.2x��3="0.2��0.5?" ?��
���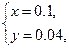 ���Եõ�CuΪ0.04��64="2.56" g ���Եõ�CuΪ0.04��64="2.56" g
�����Ѷȣ���
2������� (8��)��ش����и��ʣ�
��1�������pH��Χ��?���ڿ�����������ĸ���ָ�����п�������������?��
��2��ʯ�ҷ���ĿǰӦ����㷺�Ĺ�ҵ�����������������£�ͨ������ʯ��ʯ�õ���ʯ�ң�����ʯ��Ϊ���������������������е�SO2��Ӧ������̶���д����Ӧ�Ļ�ѧ����ʽ?��
��3������ͭ���Ʊ�Cu-Zn-Alϵ��������Ҫԭ�ϣ���ҵ����ϴ���ķ�ͭм��ԭ�����Ʊ�����ͭ�������Ʊ��������ϡ���ɫ��ѧ��˼�����?������ţ���
�� Cu + HNO3��Ũ���� Cu(NO3)2
�� Cu + HNO3��ϡ���� Cu(NO3)2
�� Cu 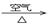 ?CuO ?CuO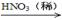 ?Cu(NO3)2? ?Cu(NO3)2?
��4����100mL 18mol��L-1��Ũ�����м��������ͭƬ������ʹ֮��ַ�Ӧ�������������ڱ�״���µ����������?��
A��40.32L
B��30.24L
C��20.16L
D��13.44L
| ��5��ijͬѧ�����ͭƬ��ϡ�����м���H2O2��ͭƬ�ܽ⣬���Ҹ÷�Ӧ�IJ���ֻ���Ȼ�ͭ��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣�����8�֣�
��1��pH��7 (1��) ?SO2? NO2(1��)
��2��Ca CO3 CaO + CO2��(1��)��Ca SO3 CaO + SO2(1��)
��3����(1��)?
��4��D (2��)
(5)Cu+2HCl+H2O2==CuCl2+2H2O(1��)
�����������
�����Ѷȣ�һ��
3������� ���Ρ��������ڹ�ũҵ�����������ˮ�����ȷ������ż���㷺��Ӧ�á�
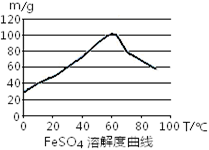
��1������м��ϡ���ᷴӦ�Ʊ�FeSO4
���Ʊ�ԭ�������ӷ���ʽ��ʾΪ?����Ҫ���FeSO4�������ʣ���ȡ���д�ʩ����ȷ����?��
A��ʹ��Ũ��������м��Ӧ?
B��ʹ��ĥϸ�����۷�Ӧ
C�������¶���50��70��?
D�������¶���80��100��
����������Ӧ�����У�������淢����Ӧ��4Fe2++O2+4H+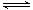 4Fe3++2H2O? 4Fe3++2H2O?
��Ҫ���ٲ�ƷFeSO4��Fe3+�ĺ�������ȡ���д�ʩ����ȷ����?��
A������ϡ�����Ũ�Ȳ���̫��?
B����ȥO2����ˮע��Ũ�������Ʒ�Ӧ�����ϡ����
C����Ӧ�б���n(Fe)/n(H2SO4) >1?
D����Ӧ��Ӧ��������Fe2��SO4��3����
�۷�Ӧ��������Һ����?����ȴ�����ˡ�ϴ�Ӽ���FeSO4��7H2O���塣
��2����ҵ���ú�������Cu��Al�ķ���м�Ʊ�Fe2��SO4��3
�䷴Ӧ�������������£�
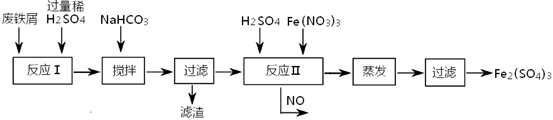
�ټ���NaHCO3�����裬�����ҺpH������?��Χ�ڣ�ʹ���ʳ������˳�ȥ��
������
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
| Cu(OH)2
| ��ʼ����
| 2.3
| 7.5
| 3.4
| 4.7
| ��ȫ����
| 3.2
| 9.7
| 4.4
| 6.7
|
?
�ڷ�Ӧ���з�Ӧ�����ӷ���ʽ�ǣ�?��
�������У�����Ӧ�������NO���һ������X����Ϻ�����ͨ�뷴Ӧ���У�����Ƶ�Ŀ����?������X��NO��ȵı�����?��
��3����Fe2��SO4��3������S2-��ˮʱ���к�ɫ����������ɫ������������䷴Ӧ�����ӷ���ʽ��?��
�ο��𰸣���1����? Fe+2H+=Fe2++H2��? B��C?��? A��C?��?����?��2����? 6.7��7.5
��? 3Fe2++NO3-+4H+ =3Fe3++NO��+2H2O?��?��ԼFe(NO3)3����ֹNO��Ⱦ? 3 : 4?
��3��2Fe3++3S2-? ="2" FeS��+S
�����������1�����������ӷ����û���Ӧ�Ʊ���������������ʹ����������Ӵ�������ӿ����ʣ�B��ȷ�����Dz�����Ũ���ᣬ���ڳ�����������Ũ����ۻ���A��������������60��ʱ�ܽ�ȸߣ�����ѡ���¶���50��70�棬C��ȷ��D������Fe2+����������������Ũ�ȣ�����H+Ũ�ȣ�ƽ�������ƶ���A��ȷ��B��ϡ��Ũ����Ӧ�ð�������ˮ�мӣ������Ͻ��裬����C�����������Է�ֹFe2+����������ȷ��D������Fe3+��������Fe3+Ũ�ȣ�����Ӧ�������˳�ȥ�����������ٽ����¶ȣ������������ܽ�ȼ�С���������塣(2)����м���������ϡ���ᣬ�������ܽ⣬ͭ���ܣ��ټ�NaHCO3��PH��6.7��7.5֮�䣬Al3+��Cu2+�������ٹ��ˣ�������������Fe2+�����������ᾧ�ò��Ϊ�˽�ԼFe(NO3)3����ֹNO��Ⱦ����������������NO����3:4��Ӧ������������������
�����Ѷȣ�����
4��ѡ���� ��ë��պȡ����30%FeCl3��Һ��ͭƬ��д��һ����Cu��������һ��ʱ�䣬������ˮ��ͭƬ�ϵ���Һ�嵽С�ձ��У�����˵������ȷ���ǣ� ? ��
A���ձ��е���Һ���ػ�ɫ
B��ͭƬ���κα仯
C��ͭƬ���а��ݵġ�Cu����
D�������ķ�ӦΪCu+Fe3+�TCu2++Fe2+
�ο��𰸣�C
���������
�����Ѷȣ���
5��ʵ���� ijͬѧ������ͼ��ʾ��ʵ��װ�ý�������ˮ������Ӧ��ʵ�飬�������о������仯����IJ������ʡ�
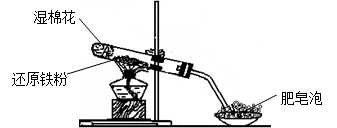
��ش��������⣺
��1��Ӳ���Թ��з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��2����ͬѧ��ȷ����Ӧ��Ӳ���Թ��й������ʵijɷ֣����������ʵ�鷽����
�ٴ�Ӳ���Թ���ȴ��ȡ���������������Թ��У������Թ��м�ϡ�������ҺB��
��ȡ������ҺB���Թ��У��μӼ���KSCN��Һ�������Һδ���ɫ��˵��Ӳ���Թ��й������ʵijɷ��У�____________________________�����ѧʽ��
��3����ͬѧ������ȡ������ҺB��ʹ���NaOH��Һ��Ӧ������ͼ
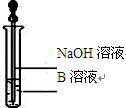
��ʾ�IJ������ɹ۲쵽�����ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��������д��������������صķ�Ӧ�Ļ�ѧ����ʽ��
��?;
��?��
��4��һ��ʱ���ͬѧ���֣�2����δ������Һ��ɺ�ɫ��˵��Fe2+ ����?�ԡ��ɴ˿�֪��ʵ������FeSO4��ҺҪ��ʱ���Ʋ����������۵�ԭ����?���������ӷ���ʽ��ʾ��
�ο��𰸣���1��3Fe+4H2O(g)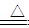 Fe3O4+4H2��2�֣�?��2��Fe3O4��Fe��2�֣� Fe3O4+4H2��2�֣�?��2��Fe3O4��Fe��2�֣�
��3��FeSO4+2NaOH==Na2SO4+2Fe(OH) 2��?��2�֣�
4Fe(OH) 2+ O2+2H2O==4Fe(OH) 3?��2�֣�
��4����ԭ��2�֣���2Fe3++ Fe==3Fe2+ ��2�֣�
�����������1������Ϊ����ˮ�����ķ�Ӧʵ�飬Ӳ���Թ��з�����Ӧ�Ļ�ѧ����ʽΪ��
3Fe+4H2O(g)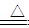 Fe3O4+4H2����2���μӼ���KSCN��Һ�������Һδ���ɫ��˵������Һ�в�û�������ӣ�˵�������ӱ�����ԭΪ�������ӣ����Թ������ʵijɷ�ΪFe3O4��Fe����3��B��Һ�к����������ӣ����Լ���NaOH��Һ�������˰�ɫ�����������������������������������ȶ������ڿ������ܹ�������Ϊ���ɫ����������������������صķ�Ӧ�Ļ�ѧ����ʽΪ��FeSO4+2NaOH==Na2SO4+2Fe(OH) 2����4Fe(OH) 2+ O2+2H2O==4Fe(OH) 3 ����4��һ��ʱ���ͬѧ���֣�2����δ������Һ��ɺ�ɫ��˵���������ӵ����ɣ�����˵�����������Ӿ��л�ԭ�ԣ�����ʵ������FeSO4��ҺҪ��ʱ���Ʋ����������۵�ԭ����Ϊ�˷�ֹ�������ӱ������������ӷ���ʽΪ2Fe3++ Fe==3Fe2+ �� Fe3O4+4H2����2���μӼ���KSCN��Һ�������Һδ���ɫ��˵������Һ�в�û�������ӣ�˵�������ӱ�����ԭΪ�������ӣ����Թ������ʵijɷ�ΪFe3O4��Fe����3��B��Һ�к����������ӣ����Լ���NaOH��Һ�������˰�ɫ�����������������������������������ȶ������ڿ������ܹ�������Ϊ���ɫ����������������������صķ�Ӧ�Ļ�ѧ����ʽΪ��FeSO4+2NaOH==Na2SO4+2Fe(OH) 2����4Fe(OH) 2+ O2+2H2O==4Fe(OH) 3 ����4��һ��ʱ���ͬѧ���֣�2����δ������Һ��ɺ�ɫ��˵���������ӵ����ɣ�����˵�����������Ӿ��л�ԭ�ԣ�����ʵ������FeSO4��ҺҪ��ʱ���Ʋ����������۵�ԭ����Ϊ�˷�ֹ�������ӱ������������ӷ���ʽΪ2Fe3++ Fe==3Fe2+ ��
���������⿼���������仯����ÿ����Ǹ߿�������ص���ȵ㣬���⿼��Ļ����϶��ǿα��ϵ�֪ʶ�������Ѷ����С�
�����Ѷȣ�һ��
|