1、填空题 实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4・7H2O),主要工艺流程如下。
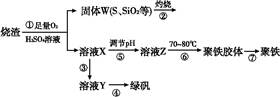
(1)将过程②产生的气体通入下列溶液中,溶液会褪色的是 。
A.品红溶液?B.紫色石蕊试液
C.酸性KMnO4溶液? D.溴水
(2)过程①中,FeS、O2和H2SO4反应的化学方程式为?。
(3)过程③中需加入的物质是 ?。
(4)过程④中,蒸发结晶时需使用的仪器除酒精灯、三脚架外,还需要?。
(5)过程⑤调节pH可选用下列试剂中的 (填序号)。
A.稀硫酸? B.CaCO3? C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70~80 ℃,目的是 ?。
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.700 0 g样品;②将样品溶于足量的盐酸后,加入过量的BaCl2溶液;③过滤、洗涤、干燥,称重得固体质量为3.495 0 g。若该聚铁的主要成分为[Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为 。(假设杂质中不含铁元素和硫元素)
参考答案:(1)ACD
(2)4FeS+3O2+6H2SO4 2Fe2(SO4)3+6H2O+4S
2Fe2(SO4)3+6H2O+4S
(3)Fe
(4)蒸发皿、玻璃棒
(5)C
(6)促进Fe3+的水解
(7)31.1%
本题解析:SO2具有漂白性,能使品红溶液褪色,SO2有还原性,能被酸性KMnO4溶液、溴水氧化,而使它们褪色。溶液X为Fe2(SO4)3,需加入还原剂将Fe3+还原为Fe2+,又不带入杂质离子,故需加入铁粉。过程⑤中需将酸消耗而调高pH,而CaCO3跟硫酸反应会生成微溶于水的CaSO4而阻止反应的继续进行。由聚铁的化学式可知:n(Fe3+)=n(S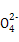 )=
)=
n(BaSO4)=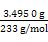 ="0.015" mol,所以聚铁样品中铁元素的质量分数=
="0.015" mol,所以聚铁样品中铁元素的质量分数=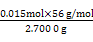 ×100%≈31.1%。
×100%≈31.1%。
本题难度:困难
2、选择题 有一种铁的氧化物样品,用5mol/L盐酸200mL恰好完全溶解,所得溶液还能吸收标况下2.24L氯气,恰好使其中Fe2+全部转化成Fe3+,该样品可能的化学式是( )
A.Fe2O3
B.Fe3O4
C.Fe4O5
D.Fe5O7
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是( )
A.Fe分别与氯气和稀盐酸反应所得氯化物相同
B.K、Zn分别与不足量的稀硫酸反应所得溶液均呈中性
C.Li、Na、K的原子半径和密度随原子序数的增加而增大
D.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
参考答案:A.Fe分别与氯气和稀盐酸反应所得氯化物为氯化铁、氯化亚铁,故A错误;
B.K、Zn分别与不足量的稀硫酸反应所得溶液分别显中性、酸性,故B错误;
C.Li、Na、K的原子半径随原子序数的增加而增大,Li、Na、K的密度随原子序数的增加先减小后增大,故C错误;
D.C、P、S、Cl的非金属性增强,则最高价氧化物对应水化物的酸性逐渐增强,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 往CuO和铁粉的混合物中,加入一定量的稀H2SO4并微热,当反应停止后,滤出不溶物,并向溶液 中插入一枚铁钉,片刻后,取出铁钉,发现铁钉并无变化,下面结论正确的是
中插入一枚铁钉,片刻后,取出铁钉,发现铁钉并无变化,下面结论正确的是
A.不溶物一定是铜
B.不溶物一定是铁 
C.不溶物 中一定含铜,但不一定含铁
中一定含铜,但不一定含铁
D.溶液中一定含有FeSO4,可能含有CuSO4
参考答案:C
本题解析:略
本题难度:一般
5、填空题 铁是一种化学性质比较活泼的金属,也是用途最广泛 的金属。铁在一定条件下能跟多种物质发生化学反应。完成下列问题:
(1)以铁为研究对象,仿照下图中的实例在框图处填写物质的化学式(所填写的反应物不属于同一类别的物质,生成物必须填写铁的化合物)。
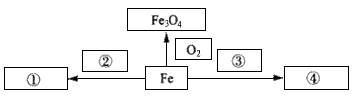
?①____;②___;③____;④____。
(2)实验室要除去细碎铜屑中的少量铁屑,请用化学方法和 物理方法将其除去。(只用简单的原理描述即可) 化学方法:___ 。物理方法:____。
(3)据统计,每年锈蚀的钢铁约占世界钢铁年产总量的四分 之一。联系生活、生产实际,举出防止钢铁生锈的两种常用方法: ①________; ②________。
(4)经研究发现,长期使用铁锅炒菜做饭,可有效地减少缺铁性贫血的发生,原因是___; 如果在炒菜时经常加入适量的食用醋,效果会更好,理由是____。
参考答案:(1)①FeCl2 ;②HCl ;③CuSO4 ;④FeSO4
(2)加入足量稀盐酸,铁会溶解在稀盐酸中,2HCl+ Fe= FeCl2+H2↑ ;用磁铁吸引铁屑
(3)①在钢铁制品表面刷油漆或镀上一层其他金属;
②保持钢铁制品表面的干燥
(4)用铁锅炒菜,会有微量的铁元素进入食物中,可补充人体需要的铁元素 ;铁能溶解在食醋中
本题解析:
本题难度:一般