1������� ��ѧ�������������ͷ�չ�Ĺ���֮һ�����ƺͷ����˸��ֲ��ϣ���������������������в��ɻ�ȱ����Ҫ���ϣ��������ѧ�����йؽ�����֪ʶ���ش��������⣺
��1��ͭǮ���ҹ���ʷ��������һ�ֹ㷺��ͨ�Ļ��ң�ͭ������������ҵ�ԭ�������______��
A��ͭ���۵㲻��̫�ߣ�����ұ�����������B��ͭ�����ʲ����ã����ױ���ʴ
C���ҹ������������ʪ��ұ��ͭ�ļ���D����Ȼ���д���������̬��ͭ
��2������Ʒ��Ϊ�������γ����ܵ���������Ĥ���������ã����Ǹ�����Ĥ�ױ�����ƻ�������������������������Һ���ã���Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣���1��A��ͭ���۵㲻��̫�ߣ�����ұ����������ͣ���Ӧ����������ң���A��ȷ��
B��ͭ�����ʲ����ã���������е�ˮ�����ȷ�Ӧ�����ױ���ʴ����B��ȷ��
C���ҹ������������ʪ��ұ��ͭ�ļ���������Fe������ͭ��Ӧ����Cu����C��ȷ��
D����Ȼ���д���ͭ���ɺ�����Cu����D����
�ʴ�Ϊ��ABC��
��2��������������������Һ��Ӧ����ƫ�����ƺ�ˮ���÷�ӦΪAl2O3+2NaOH�T2NaAlO2+H2O���ʴ�Ϊ��Al2O3+2NaOH�T2NaAlO2+H2O��
���������
�����Ѷȣ�һ��
2��ѡ���� þ������ͭ���ֽ�����ĩ����������������ַ�Ӧ�����˺�����Һ�м�������ռ���Һ���ٹ��ˣ���Һ�д��ڵ�������
[? ]
A��Mg2+
B��Cu2+
C��Al3+
D��AlO2-
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ʵ���� ѧϰС���ijƷ��������Ħ�����ɷּ��京����������̽����
������ϣ� ������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ���������ɡ�
��Ħ���������������Ķ��Լ��飺?ȡ����������Ʒ����ˮ���衢���ˡ�
��1���������м������NaOH��Һ�����ˡ�����������NaOH��Һ��Ӧ�����ӷ���ʽ��______________��
��2������1��������Һ����ͨ�����������̼���ټ������ϡ���ᡣ�۲쵽��������________________��
��������Ʒ��̼��ƵĶ����ⶨ��������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������
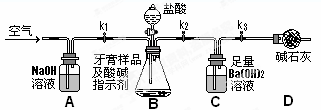
����ʵ����̻ش��������⣺
��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬����______
��4��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��__________________________
��5�����и����ʩ�У�������߲ⶨȷ�ȵ���_________�����ţ���
A���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壻?
B���μ�����˹��죻
C����A��B֮������ʢ��Ũ�����ϴ��װ��?
D����B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
��6��ʵ����ȷ��ȡ8.00g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94g������Ʒ��̼��Ƶ���������Ϊ_________��
��7��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����______________��
�ο��𰸣���1�� Al(OH)3+OH-=AlO2-+2H2O����2��ͨ��CO2�����а�ɫ�������ɣ�������������������ɣ������ܽ⣻��3�������ɵ�CO2����ȫ������C�У�ʹ֮ȫ����Ba(OH)2��Һ���գ���4��CO2+Ba(OH)2=BaCO3��+H2O����5��C,D����6��25%����7��B�е�ˮ�������Ȼ����װ������C�С�
�����������1�� ����������NaOH��Һ��Ӧ�����ӷ���ʽ��Al(OH)3+OH-=AlO2-+2H2O����2����1��������Һ�к�NaOH��NaAlO2������1��������Һ��,ͨ�����������̼�����ȷ�����Ӧ��2NaOH+CO2=Na2CO3+H2O,Ȼ������CO2++2H2O +NaAlO2= Al(OH)3+ NaHCO3; Na2CO3+H2O+CO2="2" NaHCO3;�ټ������ϡ����,�ᷢ����Ӧ��Al(OH)3+3HCl=AlCl3+3H2O ��NaHCO3+HCl=NaCl+H2O+ CO2�������Ի�۲쵽������ͨ��CO2�����а�ɫ�������ɣ�������������������ɣ������ܽ⣻��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���о��ǰ����ɵ�CO2����ȫ������C�У�ʹ֮ȫ����Ba(OH)2��Һ���գ���4��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��CO2+Ba(OH)2=BaCO3��+H2O����5��A���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壻���Լ���װ�õĿ����е�CO2���������Ӱ�죬��Сʵ��������B���μ��������Ϳ���ʽ���������屻��ֵ����գ�������Ե�ȷ�ԣ�����C����A��B֮������ʢ��Ũ�����ϴ��װ�ã�ֻ������ˮ�֣����ں�ߵ�װ���е��������վ�������Һ�н��еģ����Բ���Ӱ��ⶨȷ�ȣ���ȷ��D����B��C֮������ʢ�б���̼��������Һ��ϴ��װ�ã�����ʹװ��B�ӷ�����HCl�����ն�����CO2���壬ʹCO2�������࣬���ʹ�ⶨȷ�Ƚ��ͣ���ȷ����6������CԪ���غ�ɵù�ϵʽ��CaCO3��CO2��BaCO3��n(BaCO3)=3.94g��197g/mol=0.02mol,��n(CaCO3)=0.02mol������m(CaCO3)=0.02mol��100g/mol=2g������Ʒ��̼��Ƶ���������Ϊ��2��8����100%25%����7��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����B�е�ˮ�������Ȼ����װ������C�У���������������ƫ��
�����Ѷȣ�һ��
4������� ��0.1molþ�����Ͻ�����100mL2mol/L��H2SO4��Һ�У�Ȼ��μ�1mol/L��NaOH��Һ�����ɳ���������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
��1������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ��V��NaOH��=______mL��
��2����V1=160mLʱ��������ĩ��þ�����ʵ���Ϊ���٣���ʱV2��ֵ���Ƕ��٣�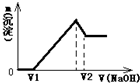
�ο��𰸣���þ�����Ͻ�����H2SO4��Һ�У�������Ӧ��Mg+H2SO4=MgSO4+H2����2Al+3H2SO4=Al2��SO4��3+3H2����0.1molþ�����Ͻ���ȫ��Ӧ��Ҫ���᷶Χ��0.1mol��n��H2SO4����0.15mol��H2SO4��ʣ�ࣨ�۲�ͼ������ó�������Һ��MgSO4��
Al2��SO4��3��H2SO4���Һ��
��0--V1�Σ��μӵ�NaOH�����к�ʣ���H2SO4��������Ӧ�ǣ�H2SO4+2NaOH=Na2SO4+2H2O
��V1mlʱ��ʣ���H2SO4��μӵ�NaOHǡ����ȫ��Ӧ����Һ��MgSO4��Al2��SO4��3��Na2SO4���Һ��
��V1--���������Σ������μӵ�NaOH��MgSO4��Al2��SO4��3��Ӧ������������������Ӧ��
Al2��SO4��3+6NaOH=2Al��OH��3��+3Na2SO4��MgSO4+2NaOH=Mg��OH��2��+Na2SO4
�ܳ��������ʱʱ��MgSO4��Al2��SO4��3��ȫ��Ӧ�������ﵽ���ֵ����ʱ����Һ��Na2SO4��Һ��
�ݳ��������--V2ml�Σ������μӵ�NaOH��Al��OH��3��Ӧ����������ʼ���٣�������Ӧ��Al��OH��3+NaOH=NaAlO2+2H2O
��V2mlʱ��Al��OH��3��ȫ��Ӧ��������Mg��OH��2����Һ��Na2SO4��NaAlO2���Һ��
��1������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ���������ﵽ���ֵ����ʱ����Һ��Na2SO4��Һ������SO42-���Ӻ�Na+�����غ��У�n��Na+��=2n��Na2SO4��=2n��H2SO4��=2��0.1L��2mol/L=0.4mol�����ԣ���ʱ��V��NaOH��=0.4mol1mol/L=0.4L=400ml
�ʴ�Ϊ��400��
��2����V1=160mLʱ����ʱ����Һ��MgSO4��Al2��SO4��3��Na2SO4���Һ��
��Na+�����غ��֪��n��Na2SO4��=12n��Na+��=12n��NaOH��=12��0.16L��1mol/L=0.08mol
��MgSO4Ϊxmol��Al2��SO4��3Ϊymol������Mgԭ�ӡ�Alԭ�ӡ�SO42-�����غ��У�
���������
�����Ѷȣ�һ��
5��ѡ���� ����MgCl2��AlCl3�������ʵĻ����Һ����εμ�7mLNaOH��Һ������εμ����������ٷ�����ѧ��Ӧ�����ó��������ʵ���Y�������Լ������V֮��Ĺ�ϵ��ͼ��ʾ�����½��۴������(������Mg2+��Al3+��ˮ��)?
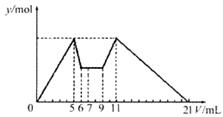



A������NaOH��Һ��HCl��Һ�����ʵ���Ũ��֮��Ϊ2��1
B��ԭ�����Һ��c(Al3+)��c(Mg2+)��c(Clһ)=1��1��5
C���������HCl��Һ�����Ϊ4mLʱ����Һ��c(Na+)��c(C1һ)=1��2
D�����յõ�����Һ��c(A13+)��c(Mg2+)��c(Cl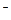 )=1��1��14
)=1��1��14
�ο��𰸣�CD
����������������HCl��Һ�����Ϊ11��7=4mLʱ��������ﵽ���������Һ������ֻ��NaCl������Һ��c(Na+)��c(Cl )=1��1��������Һ��c(A13+)��c(Mg2+)��c(C1
)=1��1��������Һ��c(A13+)��c(Mg2+)��c(C1 )=1��1��12��
)=1��1��12��
�����Ѷȣ�һ��