1、选择题 下列陈述I、II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II
A
浓H2SO4有吸水性
浓H2SO4可用于干燥氨气
B
SO2有氧化性
SO2尾气可用NaOH溶液吸收
C
Mg有还原性
电解MgCl2饱和溶液可制备Mg
D
锌金属活动性比铁强
海轮外壳上装锌块可减缓腐蚀
|
A.A
B.B
C.C
D.D
2、选择题 相同质量的Mg与Al,分别与足量的稀盐酸反应,产生H2(标准状况下)的体积比为(?)
A.3:4
B.1:3
C.8:9
D.4:3
3、选择题 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是
①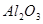 ;②
;②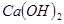 ;③
;③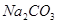 ;④
;④
A.①②
B.②③
C.①④
D.③④
4、选择题 下列关于金属铝的叙述不正确的是
[? ]
A.铝是地壳中含量最多的金属元素
B.铝是比较活泼的金属,在化学反应中容易失去电子,表现出还原性
C.铝箔在空气中用酒精灯加热可以熔化,且发生剧烈燃烧
D.铝箔在空气中用酒精灯加热可以熔化,由于氧化膜的存在,熔化的铝并不滴落
5、填空题 (16分)镁化合物和氯气均具有广泛用途,请回答下列问题:
(1)写镁和氯气反应产物的电子式?
(2)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是?
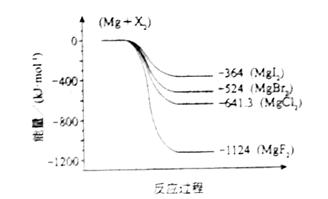
A? MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B? Mg与X2的反应是放热反应
C? MgBr2与Cl2反应的△H<0
D?化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
(3)在298K、100Kpa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
①该反应的离子方程式为?,平衡常数表达式为?
②在上述平衡体系中加入少量NaCl固体,平衡将?(填“正向移动”、“逆向移动”、“不移动”);增大氯气的压强,氯气的溶解度将??,氯气和水反应的平衡常数将?
?(填“变大”、“变小”、“不变”)。
③已知:? H2CO3 ?HCO3- + H+?Ka1(H2CO3) = 4.45×10-7 ?
?HCO3- + H+?Ka1(H2CO3) = 4.45×10-7 ?
HCO3- CO32- + H+?Ka2(H2CO3) = 5.61×10-11
CO32- + H+?Ka2(H2CO3) = 5.61×10-11
HClO  ?H+ + ClO-?Ka(HClO) = 2.95×10-8
?H+ + ClO-?Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;