1、填空题 向20 mL AlCl3溶液中滴入2 mol・L-1 NaOH溶液时,得到Al(OH)3沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:

(1)图中A点表示的意义是___________________________________________________。
(2)图中B点表示的意义是___________________________________________________。
(3)上述两步用总的离子方程式可表示为________________________。
(4)假若溶液中有Al(OH)3沉淀0.39 g,则此时用去NaOH溶液体积为______________。
参考答案:(1)表示滴入NaOH溶液产生沉淀量最大点
(2)表示滴入NaOH溶液沉淀恰好完全溶解点
(3)Al3+?+4OH-====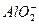 +2H2O
+2H2O
(4)7.5 mL或17.5mL
本题解析:把NaOH溶液滴入AlCl3溶液中,先产生Al(OH)3沉淀,其质量最大值(A点),然后全部消失溶解(B点)。其总的反应离子方程式为:
Al3++4OH-====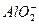 +2H2O
+2H2O
当有0.39 g Al(OH)3沉淀生成时,①AlCl3过量,加入NaOH使Al3+部分产生沉淀0.39 g,通过Al3++3OH-====Al(OH)3可知用NaOH7.5 mL。②当NaOH过量使Al3+全部参加反应生成Al(OH)3沉淀后又部分溶解,用NaOH 17.5 mL。
本题难度:简单
2、填空题 用镁铝合金的废料头、稀硫酸、氢氧化钠溶液制取MgCl2溶液和Al2(SO3)3溶液,只需通过四步反应完成,请依次写出其化学方程式:
(1)____________________________________。
(2)_______________________?_________。
(3)____________________________________。
(4)___________________________?_____。
参考答案:(1)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(2)2NaAlO2+H2SO4+2H2O=Na2SO4+2Al(OH)3↓
(3)2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
(4)Mg+2HCl=MgCl2+H2↑
本题解析:首先要利用镁和铝的性质不同,将镁和铝分离开,然后再按照要求通过一定化学反应制备目标产物。所利用的反应规律在初中化学里同学们已经学过了,此处实际也是一个复习过程。
本题难度:简单
3、选择题 下列叙述中所描述的物质一定是金属元素的是( ?)
A.易失去电子的物质
B.原子最外层只有一个电子的元素
C.单质具有金属光泽的元素
D.第3周期中,原子最外电子层只有2个电子的元素
参考答案:D
本题解析:A中H不符合,B中可能为H,C中可能为石墨,均不符合题干要求。
本题难度:简单
4、选择题 下列各金属的混合物2.5 g和足量的盐酸反应,放出的H2在标准状况下体积为2.24 L,其中可能的是(? )
A.Zn和Fe
B.Mg和Zn
C.Al和Mg
D.Cu和Fe
参考答案:B
本题解析:假设2.5 g分别是Zn、Fe、Mg、Al,看生成H2比2.24 L多还是少,再据同质量金属与酸反应产生H2量顺序Al>Mg>Fe>Zn判断。
本题难度:简单
5、实验题 设计实验探讨向AlCl3溶液中加入过量的NaOH和向NaOH溶液中加入过量的AlCl3现象是否一样。_________________________________
参考答案:向AlCl3溶液中逐滴加入NaOH有白色沉淀生成,当NaOH过量时沉淀溶解,最后生成物为NaAlO2。反应的离子方程式为:Al3++3OH-==Al(OH)3↓,Al(OH)3+OH-==?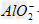 +2H2O
+2H2O
向NaOH溶液中逐滴加入AlCl3溶液时,观察到的现象是:开始有白色沉淀生成,振荡后立即消失,继续滴加AlCl3溶液直至过量时,又出现白色沉淀,且不消失。这是因为反应开始时,由于NaOH溶液过量,滴入的AlCl3和NaOH作用转化为NaAlO2,当加入过量AlCl3时,AlCl3和NaAlO2在溶液里发生反应,生成沉淀Al(OH)3。其反应的离子方程式为:Al3++3OH-====Al(OH)3↓,Al(OH)3+OH-==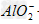 +2H2O,Al3++3
+2H2O,Al3++3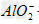 +6H2O==4Al(OH)3↓
+6H2O==4Al(OH)3↓
综上所述,二者滴加顺序不同,现象不一样。
本题解析:
本题难度:一般