1、选择题 化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提高化
学反应的限度,下面的说法错误的是
A.能够节约原料和能源
B.能够提高产品的产量
C.能够提高经济效益
D.能够提高化学反应速率
参考答案:D
本题解析:略
本题难度:一般
2、选择题 下列有关工业生产叙述正确的是( )
A.工业上通常使用电解法制备金属钠、镁、铝等
B.合成氨工业中,将NH3及时液化分离有利于加快反应速率
C.硫酸工业中,采用常压条件的原因是此条件下催化剂活性最高
D.电解精炼铜时,将粗铜与电源的负极相连
参考答案:A、活泼金属冶炼是利用电解熔融的金属氯化物得到,故A正确;
B、合成氨工业中,将NH3及时液化分离,浓度减小,速率减小,故B错误;
C、常采用常压条件的原因是,压条件二氧化硫的转化率易很大,加压转化率增大不大,故C错误;
D、电解精炼铜时,将粗铜与电源的正极相连,做电解池的阳极,失电子发生氧化反应,故D错误;
故选A.
本题解析:
本题难度:简单
3、选择题 F2、Cl2、Br2、I2分别与H2反应在相同的条件下.活化分子物质的量分数最大的是( )
A.F2+H2=2HF
B.Cl2+H2=2HCl
C.Br2+H2=2HBr
D.I2+H2=2HI
参考答案:非金属性:F>Cl>Br>I,元素的非金属性越强,对应的单质越活泼,与氢气反应越剧烈,活化分子物质的量分数越大,则反应F2+H2=2HF中活化分子物质的量分数最大,
故选A.
本题解析:
本题难度:一般
4、填空题 在200℃时,将amolH2(g)和bmolI2(g)充入到体积为VL的密闭容器中,发生反应:
I2(g)+H2(g)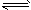 2HI(g)
2HI(g)
(1)反应刚开始时,由于C(H2)=_______,C(I2)=_______,而C(HI)=_______,所以化学反应速率_______最大,而_______最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为C(H2)_______,C(I2)_______,而
C(HI)_______,从而化学反应速率ν(正)_______,而ν(逆)_______。
(3)当反应进行到ν(正)与ν(逆)_______时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将_______。
参考答案:(1)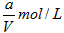 ;
;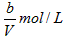 ;0;ν(正);ν(逆)
;0;ν(正);ν(逆)
(2)减小;减小;增大;减小;增大
(3)相等;保持不变
本题解析:
本题难度:一般
5、选择题 一定量的稀硫酸跟过量铁粉反应,为了减缓反应速率,又不影响生产氢气的总量,可向稀硫酸中加入适量的
[? ]
A.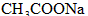 (固体)
(固体)
B.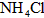 (固体)
(固体)
C.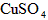 (溶液)
(溶液)
D.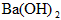 (固体)
(固体)
参考答案:A
本题解析:
本题难度:一般