1、选择题 下列操作达不到目的的是
①石油分馏时把温度计插入受热的液体中②用酸性高锰酸钾溶液除去乙烯中含有的H2S③用乙醇和3%的硫酸共热到170℃制乙烯 ④将苯和溴水混合后加入铁粉制取溴苯⑤将醋酸钠晶体和碱石灰混合共热制甲烷
A.①⑤
B.③④⑤
C.③⑤
D.①②③④⑤
参考答案:D
本题解析:略
本题难度:一般
2、实验题 设计实验证明盐酸和NaOH溶液发生了反应。学生提出了许多有创意的想法:①用酸碱指示剂监测,②用pH试纸监测,③利用导电实验测定离子浓度的变化,④将盐酸和碱液混合后的溶液蒸干后品尝味道。请对上述创意作出评判后回答下列问题:
⑴在想法①中,如果是将NaOH溶液滴入盐酸中,可以在盐酸中先加几滴____(填一种酸碱指示剂的名称),再不断滴入NaOH溶液,颜色由__?_?变___?__。
⑵在想法②中,写出测定pH的基本操作:___________________?_。
⑶在想法③中,如用浓度均为1mol/L的盐酸和NaOH溶液进行实验,简述实验的操作步骤,并说明是如何判断盐酸与NaOH溶液发生了反应。
⑷对第④中设计,提出你的看法?
⑸你能否提出其它一些有创意的想法。
参考答案:⑴甲基橙,红色、黄色(或酚酞,无色、红色)⑵用洁净,干燥的玻璃棒沾取待测液滴在试纸上,用标准比色卡对照,读数。⑶连接导电性实验装置,加入盐酸观察灯泡亮度(如连接安培表,则读数);缓慢加入NaOH溶液观察灯泡亮度。如灯泡亮度变暗,表示离子浓度减小,盐酸与NaOH溶液发生了反应,如不反应,则离子浓度将不变,灯泡亮度不变。⑷不正确⑸在未加碱液和已加碱液的盐酸中放入铁粉、碳酸钠等以比较反应速率;在未加盐酸和已加盐酸的碱液中放入铝粉比较反应速率。
本题解析:⑴根据指示剂的变^色 情况,可以选用甲基橙,颜色由红色变为黄色,也可以选用酚酞,颜色由无色变为红色。⑵测定pH的基本操作:用洁净,干燥的玻璃棒沾取待测液滴在试纸上,用标准比色卡对照,读数。⑶操作步骤:连接导电性实验装置,加入盐酸观察灯泡亮度(如连接安培表,则读数);缓慢加入NaOH溶液观察灯泡亮度。如灯泡亮度变暗,表示离子浓度减小,盐酸与NaOH溶液发生了反应,如不反应,则离子浓度将不变,灯泡亮度不变。⑷肯定不正确,因为实验中的试剂是不能品尝的,况且简单地混合是很难控制两者恰好反应,如果碱过量,蒸干后碱过量会有强烈的腐蚀作用。⑸在未加碱液和已加碱液的盐酸中放入铁粉、碳酸钠等以比较反应速率;在未加盐酸和已加盐酸的碱液中放入铝粉比较反应速率。或者其它合理想法。
本题难度:一般
3、选择题 下列各组液体混合物中,不分层的是
A.苯和水
B.酒精和水
C.油和水
D.三氯甲烷和水
参考答案:B
本题解析:酒精和水能互相以任意比例互溶,所以不会分层。答案选B
本题难度:简单
4、实验题 (14分)某研究性学习小组将一定浓度的Na2CO3?溶液滴入CuSO4溶液中得到沉淀。
甲同学认为两者反应只有CuCO3一种沉淀生成;
乙同学认为这两者相互促进水解反应,生成Cu(OH) 2一种沉淀;
丙同学认为生成CuCO3和Cu(OH) 2两种沉淀。
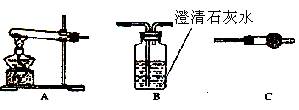
(1)各装置连接顺序为 ?→??→ ?。
(2)若甲同学的结论正确,实验现象为 ?。
II.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。

(1)仪器组装好后首先要进行的实验操作是 ?,实验结束时要继续通入处理过的过量空气,其作用是?。
(2)若沉淀样品的质量为mg,当反应完全后,装置C质量增加了ng,则沉淀中CuCO3的质量分数为?。
III.沉淀转化在生产中也有重要应用。例如,用Na2CO3溶液可以将锅炉水垢中的CaSO4转化为较疏松瓶易清除的CaCO3,该沉淀转化达到平衡时,其平衡常数K=___________(写数值)。[已知Ksp(CaSO4)=9.1×10―6,Ksp(CaCO3)=2.8×10―9]
IV.蓝铜矿的主要成分为2CuCO3・Cu(OH)2,当它与焦炭一起加热时,可以生成铜、二氧化碳和水,写出该反应的化学方程式_____________________________________________
参考答案:I、⑴A→C→B? ⑵C中无水硫酸铜不变色, 装置B中澄清石灰水变浑浊?
Ⅱ.⑴检查装置的气密性? ⑵可以将装置中滞留的水蒸气和CO2排出,使其分别被浓硫酸和碱石灰充分吸收。⑶1-49n/9m
Ⅲ.3.25×103
IV.2[2 CuCO3・Cu(OH)2]+3C=7CO2+6Cu+2H2O
本题解析:I.请用下图所示装置,选择必要的试剂,利用以下装置完成简单的定性探究生成物的成分的实验。I(1)沉淀加热分解的气体为H2O和CO2,C中干燥管吸收H2O,B中澄清石灰水吸收CO2,因澄清石灰水中含有水份,所以先吸收H2O后吸收CO2,故各装置连接顺序为A→C→B。(2)CuCO3加热分解生成的气体只有CO2,故实验现象为:C中无水硫酸铜不变色, 装置B中澄清石灰水变浑浊。
II(2)若沉淀样品的质量为m克,装置B质量增加了n克,应为水的质量,发生:Cu(OH)2 CuO+H2O,
CuO+H2O,
Cu(OH)2 CuO+H2O
CuO+H2O
98g ?18g
m(Cu(OH)2) ng
m(Cu(OH)2) ,
,
m(CuCO3) ,
,
ω(CuCO3) =1-49n/9m,
=1-49n/9m,
则沉淀中CuCO3的质量分数为1-49n/9m,
故答案为:1-49n/9m。
点评:本题考查化学反应机理的探究,题目难度中等,本题注意根据物质的化学性质设计实验方案,易错点为Ⅲ,注意实验时要排除空气中水和二氧化碳的干扰。
本题难度:困难
5、实验题 化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
Ⅰ.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水成分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是___________________________________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是_______________________________。
Ⅱ.牙膏样品中碳酸钙的定量测定利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
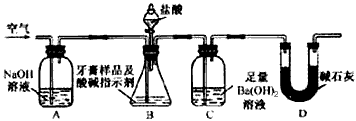
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________________。
(4)C中反应生成BaCO3的化学方程式是________________________________。
(5)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g 。则样品中碳酸钙的质量分数为_________。
参考答案:(1)Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2-+2H2O
(2)通入CO2气体有Al(OH)3白色沉淀生成,并且生成NaHCO3,加入盐酸有CO2气体产生、Al(OH)3沉淀溶解
(3)实验过程中需持续缓缓通入空气,把生成的CO2全部排入C中,使之完全被Ba(OH)2溶液吸收
(4)CO2+Ba(OH)2=BaCO3↓+H2O
(5)25%
本题解析:
本题难度:一般