1、实验题 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置先进行了有关实验:
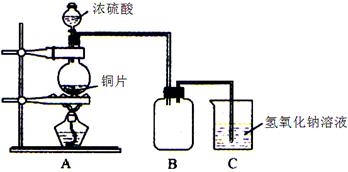
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整。
(2)实验中他们取6.4g 铜片和12mL 18mol・L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式?。
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是?。
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是?(填写编号)。
A.铁粉? B.氯化钡溶液? C.银粉? D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,甲、乙学生进行了如下设计:
①甲同学设计方案是:先测定铜与浓硫酸反应产生的SO2的量,在计算余酸的物质的量浓度。他认为测定二氧化硫的量的方法有多种,请问下列实验方案中可行的是?(填写编号)。
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案进行分析(可以不填满):
方案序号
| 分析
| 误差(偏低或偏高)
| 改变措施
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
②乙学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL与锥形瓶中,滴入2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度。假定反应前后烧瓶中溶液的体积不变,你认为乙学生设计的实验方案能否求得余酸的物质的量浓度_______(填“能”或“不能”),其理由是?。
(4)请再设计其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)?
?。
参考答案:(1)如图所示。
 (2分)
(2分)
(2)①Cu + 2H2SO4(浓) CuSO4 + SO2↑+ 2H2O(2分)
CuSO4 + SO2↑+ 2H2O(2分)
②随着反应进行,硫酸被消耗,产物有水生成,所以浓硫酸变成稀硫酸,反应会停止(1分)
③AD(1分)
(3)①E(1分)
方案序号
分析
误差(偏低或偏高)
改变措施
A
碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大
偏低
A产生的气体先经浓硫酸干燥,后用碱石灰吸收
B
高锰酸钾溶液中含有硫酸,与氯化钡反应生成沉淀增大
偏低
将硫酸酸化的高锰酸钾溶液换成溴水或碘水或硝酸溶液
C
二氧化硫在水中以1∶40溶解,收集二氧化硫体积减少
偏高
将水换成四氯化碳、煤油等非极性溶剂
D
亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大
偏低
先将二氧化硫用强氧化剂如溴水氧化,再加入足量的氯化钡溶液或氢氧化钡溶液
②不能(1分)?虽然甲基橙变色范围:pH为3.1~4.4,氢氧化铜开始沉淀时的pH为5,在指示剂变色范围之外,即中和酸时,铜离子不会消耗OH-,但是甲基橙由红色变成橙色、黄色时,铜离子溶液呈蓝色,对观察指示终点颜色有干扰。(1分)
(4)(2分)
方案一:①取反应后溶液,向其中加入足量锌;②收集并测定氢气的体积;③通过氢气量计算剩余硫酸的物质的量浓度。
方案二:①取反应后溶液,向其中加入过量的氢氧化钠溶液,至氢氧化铜完全沉淀;②过滤、洗涤、(低温)干燥、称量至恒重;③根据氢氧化铜的量计算出已反应的硫酸的量,进而计算剩余硫酸溶液浓度。
方案三:反应结束后将烧瓶中的铜片取出,洗净、烘干,称其质量即可。
方案四:反应结束后将烧瓶中的铜片取出,然后向溶液中加入足量氯化钡溶液,过滤出沉淀,洗净、干燥后称量。(只要合理即得2分)
本题解析:(1)SO2的密度大于空气的,所以通过排气法收集SO2时,应该是长进,短出。
(2)浓硫酸具有氢氧化性,在加热的条件下和铜反应生成硫酸铜、SO2和水。由于稀硫酸和铜不反应,而随着反应的进行,硫酸的浓度会逐渐降低,当降低到一定浓度后,反应就停止,所以一定有硫酸剩余。如果有硫酸剩余,则加入铁粉或碳酸氢钠后,一定会产生气体,据此可以验证。由于溶液中有硫酸铜,所以加入氯化钡一定产生白色沉淀,无法注明是否含有硫酸。银和稀硫酸及硫酸铜都不反应,所以答案是AD。
(3)A中碱石灰除了能吸收SO2外,还能吸收水蒸气,导致测得的SO2质量偏大,测得结果偏低。所以应该再通过碱石灰之前先通过浓硫酸进行干燥。B中高锰酸钾溶液中就含有硫酸,从而生成的白色沉淀质量偏大,结果偏低。高锰酸钾不能用硫酸酸化,可以用硝酸酸化。SO2易溶于水,所以测得的SO2偏低,结果偏高。可以用有机溶剂代替水。SO2和氢氧化钡反应生成的是亚硫酸钡,亚硫酸钡不稳定,在空气中易被氧化生成硫酸钡,是结果偏低。因此在通入氢氧化钡之前,要首先把SO2氧化生成硫酸,然后再和氢氧化钡反应。硝酸具有氧化性,能把SO2氧化生成硫酸,从而生成硫酸钡沉淀,所以E是正确的。
(4)由于氢氧化钠和硫酸首先反应,而硫酸铜开始是不反应的。由于铜离子在溶液中显蓝色,所以会干扰甲基橙的颜色变化,导致滴定不准确。
(5)本题属于开放性试题,只有原理正确,可操作性强均可以。具体解析见答案。
本题难度:一般
2、实验题 (8分,每空2分)实验室要配制500mL2.0mol・L-1氯化钠溶液。请回答下列问题:
(1)应用托盘天平称取NaCl固体 g;
(2)下列仪器中,配制时一定不会用到的是(填字母) ;
A.量筒?B.500 mL烧瓶
C.胶头滴管? D.500mL容量瓶
(3)除上述(2)中用到的仪器外,还缺少的玻璃仪器有 ?;
(4)右图所示是某同学配 制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响?? ?(填“偏高”、”偏低”或“无影响”);
制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响?? ?(填“偏高”、”偏低”或“无影响”);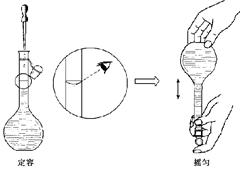
参考答案: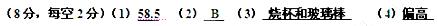
本题解析:略
本题难度:一般
3、实验题 无水FeCl3呈棕红色,极易潮解,100℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
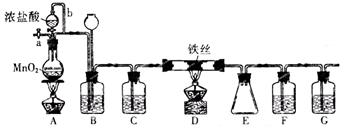
请回答:
(1)装置A中反应的离子方程式为?。
(2)装置F中所加的试剂为?。
(3)导管b的作用为?;
装置B的作用为?。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为?。
(5)反应结束后,拆卸装置前,必须进行的操作是?
(6)为检验所得产品中是否含有FeCl2,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入一种试剂,该试剂为??(填序号)。
①Fe粉?②KSCN溶液?③酸性KMnO4溶液? ④NaOH溶液
参考答案:
(1)MnO2+4H++2Cl― Mn2++Cl2↑+2H2O?(2分,反应条件不作为给分点,写成化学方程式该空不能得分。)
Mn2++Cl2↑+2H2O?(2分,反应条件不作为给分点,写成化学方程式该空不能得分。)
(2)浓硫酸或浓H2SO4(2分,不写“浓”字不给分。)
(3)平衡压强(或使浓盐酸顺利流下);(2分)
除去Cl2中的HCl气体,判断实验过程中导管是否被产品堵塞(两个要点各1分,共2分)
(4)排尽实验装置中的空气(2分)
(5)打开活塞a,通入空气把装置内残留的Cl2排出,保证吸收更彻底(其它合理答案均可)(2分)
(6)③(2分)
本题解析:该实验的思路是先制取纯净、干燥的氯气,然后让氯气与铁单质反应,考虑到无水氯化铁易潮解,应防止空气中的水蒸气进入集气瓶,在集气瓶后连接盛有浓硫酸的洗气瓶,考虑到氯气有毒,应进行尾气处理,最后用碱液吸收未完全反应的氯气。
(3)制取气体时,发生装置中产生气体使装置内压强过大,溶液导致分液漏斗中液体不能顺利流下,为防止这种现象发生,需使分液漏斗上下压强相等,导管b的作用就是使分液漏斗上下压强相等。
B中盛有饱和食盐水,除去氯气中的杂质HCl气体。生成的氯化铁升华为气体沿导管进入集气瓶,但在导管中氯化铁遇冷容易凝化为固体,可堵塞导管,这样会使装置内压强过大而产生危险,因此实验过程中必须注意导管是否堵塞;B中的长颈漏斗可帮助判断导管是否堵塞,若堵塞则B中的液体受到压强过大会进入长颈漏斗。
(4)先点燃A处酒精灯,反应一会是为了排尽装置内的空气。
(5)氯气有毒,拆装置前要将装置内残留的氯气完全排尽,通常采用的方法是向装置内通入空气。
(6)因溶液中含有Fe2+、Fe3+,因此检验时要利用Fe2+的还原性,向其中加入酸性高锰酸钾溶液,看酸性高锰酸钾是否褪色。
本题难度:一般
4、选择题 实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸镏②水洗③用干燥剂干燥④用10%的NaOH溶液洗⑤水洗。正确的操作顺序是?
A.①②③④⑤
B.②④⑤③①
C.④②③①⑤
D.②④①⑤③
参考答案:B
本题解析:生成的溴苯中含有苯和单质溴,溴苯不溶于水,溴单质苯溶于水,因此首先用水洗,然后再用氢氧化钠溶液洗,再用水洗残余的氢氧化钠等,最后通过干燥剂干燥除去多余的水。由于溴苯的沸点和苯差别很大,所以通过蒸馏即可得到溴苯。答案选B。
本题难度:简单
5、选择题 下图是制取和收集某气体的实验装置,该装置可用于
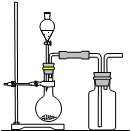
A.用浓硫酸和氯化钠反应制取HCl
B.用浓氨水和生石灰反应制取NH3
C.用双氧水与二氧化锰反应制取O2
D.用饱和食盐水和电石反应制取C2H2
参考答案:C
本题解析:该装置为固液不加热制取气体,且用向上排空气法,只有C符合。A、制取HCl需加热;B、制取氨气,采用向下排空气法收集,错误;D、乙炔制取采用排水法。
本题难度:一般