1、选择题 碱石灰和五氧化二磷均能干燥的一组气体是
A.N2、O2、NH3
B.CO、NO、H2
C.H2、NO、NH3
D.NO、Cl2、N2
2、实验题 (6分)图5是实验室制取Cl2并以Cl2为原料进行特定反应的实验:
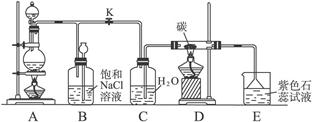
图5
(1)A为氯气发生装置,写出反应的化学方程式:_________________________________。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯,连上E装置。Cl2通过C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),试写出D装置中反应的化学方程式_______________________;装置C的作用是_________________________________。
(3)E处石蕊试液的现象是_____________________________________________________,其原因是______________________________________________________________________。
(4)若将E处溶液改为石灰水,反应过程的现象是_________________________________。
a.有白色沉淀生成
b.无白色沉淀生成
c.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________________________,B的作用是
___________________________。
3、实验题 (11分)某同学按下列步骤配制500 mL 0.2 mol・L-1 KCl溶液,请回答下列问题:
实验步骤
| 有关问题
|
(1)计算所需KCl的质量
| 需要KCl的质量为______g
|
(2)称量KCl固体
| 称量过程中主要用到的仪器有________________
|
(3)将KCl放入到100 mL烧杯中加水溶解
| 为加快溶解速度,可采取的措施是______________________
|
(4)将烧杯中的溶液转移至500 mL容量瓶中
| 为防止溶液溅出,应采取的措施是____________________
|
(5)向容量瓶中加蒸馏水到刻度线
| 在进行此操作时应注意的问题是__________________________
|
你认为按上述步骤配制的KCl溶液的浓度是否为0.2 mol・L-1,请说明理由。
4、实验题 (2分)下列实验操作或对实验事实的描述中正确的说法有?。
①如果苯酚浓溶液沾到皮肤上,应立即用酒精洗涤
②除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③实验室制硝基苯:向浓硝酸、浓硫酸的混合酸中滴入苯,在50~60℃的水浴中加热
④实验室制取乙烯时,将无水乙醇和10mol・L-1 H2SO4混合加热到1700C,可制得乙烯
⑤只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑥检验卤代烃中的卤离子,是将试样放入试管,然后加入NaOH煮沸,随即加入硝酸银即可。
5、填空题 高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如图),其实验流程如下:
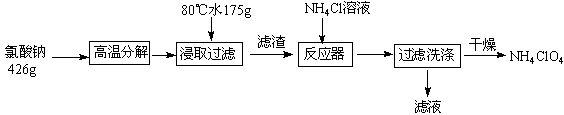
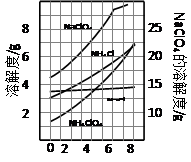
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为?。
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为?(写化学式)。
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为?。
(4)已知:2NH4ClO4  N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
a.饱和食盐水? b.浓H2SO4? c.NaOH溶液? d.Mg? e.Cu? f.Fe
利用下图装置对高氯酸铵热分解产生的三种气体进行分步吸收或收集。

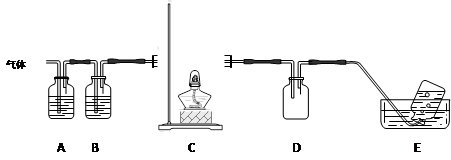
①E中收集到的气体可能是?(填化学式) 。
②装置D的作用可能是?。
③A、B、C中盛放的药品依次可以是?(选填:Ⅰ、Ⅱ、Ⅲ)。
Ⅰ. a b d?Ⅱ. c b e?Ⅲ. b c f