1、实验题 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置先进行了有关实验:
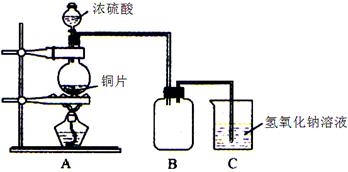
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整。
(2)实验中他们取6.4g 铜片和12mL 18mol・L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式?。
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是?。
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是?(填写编号)。
A.铁粉? B.氯化钡溶液? C.银粉? D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,甲、乙学生进行了如下设计:
①甲同学设计方案是:先测定铜与浓硫酸反应产生的SO2的量,在计算余酸的物质的量浓度。他认为测定二氧化硫的量的方法有多种,请问下列实验方案中可行的是?(填写编号)。
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案进行分析(可以不填满):
方案序号
| 分析
| 误差(偏低或偏高)
| 改变措施
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
|
②乙学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL与锥形瓶中,滴入2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度。假定反应前后烧瓶中溶液的体积不变,你认为乙学生设计的实验方案能否求得余酸的物质的量浓度_______(填“能”或“不能”),其理由是?。
(4)请再设计其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)?
?。
2、实验题 (8分,每空2分)实验室要配制500mL2.0mol・L-1氯化钠溶液。请回答下列问题:
(1)应用托盘天平称取NaCl固体 g;
(2)下列仪器中,配制时一定不会用到的是(填字母) ;
A.量筒?B.500 mL烧瓶
C.胶头滴管? D.500mL容量瓶
(3)除上述(2)中用到的仪器外,还缺少的玻璃仪器有 ?;
(4)右图所示是某同学配 制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响?? ?(填“偏高”、”偏低”或“无影响”);
制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响?? ?(填“偏高”、”偏低”或“无影响”);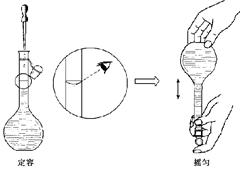
3、实验题 无水FeCl3呈棕红色,极易潮解,100℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
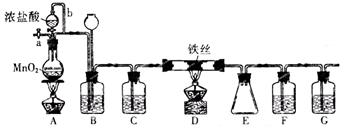
请回答:
(1)装置A中反应的离子方程式为?。
(2)装置F中所加的试剂为?。
(3)导管b的作用为?;
装置B的作用为?。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为?。
(5)反应结束后,拆卸装置前,必须进行的操作是?
(6)为检验所得产品中是否含有FeCl2,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入一种试剂,该试剂为??(填序号)。
①Fe粉?②KSCN溶液?③酸性KMnO4溶液? ④NaOH溶液
4、选择题 实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸镏②水洗③用干燥剂干燥④用10%的NaOH溶液洗⑤水洗。正确的操作顺序是?
A.①②③④⑤
B.②④⑤③①
C.④②③①⑤
D.②④①⑤③
5、选择题 下图是制取和收集某气体的实验装置,该装置可用于
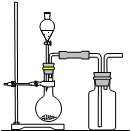
A.用浓硫酸和氯化钠反应制取HCl
B.用浓氨水和生石灰反应制取NH3
C.用双氧水与二氧化锰反应制取O2
D.用饱和食盐水和电石反应制取C2H2