1、简答题 三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料
Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加?KSCN?试剂.
(1)若假设1成立,则实验现象是______.
(2)若滴加?KSCN?试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?______.简述你的理由(可不写反应的方程式?)______.
(3)若固体粉末完全溶解无固体存在,滴加?KSCN?试剂时溶液不变红色,则证明原固体粉末是______,写出发生反应的离子方程式______.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a?g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(?b>a),则混合物中Cu2O的质量分数为______.
(5)实验小组欲利用该红色粉末制取较纯净的胆矶?(CuSO4.5H2O).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH?如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3
开始沉淀pH
6.0
7.5
1.4
沉淀完全pH
13
14
3.7
|
实验室有下列试剂可供选择:A.氯水?B.H2O2?C.NaOH?D.Cu2(OH)2CO3
实验小组设计如下实验方案:
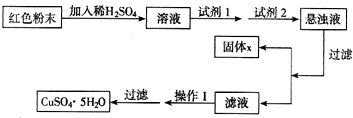
试回答:
试剂1为______,试剂2为______(填字母序号);固体x的化学式是______.
2、选择题 将Fe和Cu的混合粉末ag加入到100mL4mol/L稀硝酸中充分反应后(假设通原产物只有NO),下列说法正确的是?(?)
A.若反应后有Cu剩余,则反应后溶液中含有的金属阳离子一定是Cu2+
B.若反应后的溶液中有Cu2+,则反应后溶液中含有的金属阳离子一定是Fe2+、Fe3+
C.若反应后的溶液中无金属剩余,则加入金属粉末质量8.4 g<a<9.6 g
D.若加入的Fe和Cu的质量比为7:8,则使HN03完全反应的金属粉末质量最小为7.2 g
3、填空题 某氧化铁样品中含有少量的FeSO4杂质。某同学要测定其中铁元素的质量分数,他设计了如下方案进行测定,操作流程为:
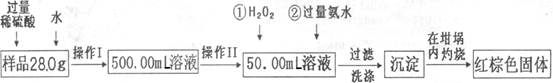
请根据流程回答:
(1)操作I中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有??(填仪器名称)。
(2)操作II中必须用到的仪器是?。
A.50mL量筒
B.100mL量筒
C.50mL酸式滴定管
D.50mL碱式滴定管