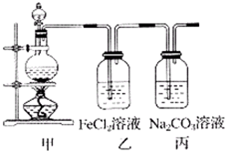
1、简答题 (1)某学习小组利用下图装置制取氯气并探究其性质.
①甲装置中反应的化学方程式是______;
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象)______;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质.已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是______.
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究.
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol?L-1盐酸、品红溶液、新制澄清石灰水.
【提出假设】假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含______;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3.
【进行实验】在答题卡上完成下表(不必检验Ca2+、Cl-):
| 实验步骤 | 预期现象和结论
①
用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管______
若无气体放出且澄清石灰水未见浑浊,则假设一成立;______
②
______
______
|
参考答案:(1)①浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,反应的化学方程式为MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O;
②氯化铁和氯气反应,2FeCl2+Cl2=2FeCl3,三价铁离子和硫氰酸钾反应生成血红色溶液,Fe3++3SCN-=Fe(SCN)3,故答案为:KSCN,溶液变为血红色;
③氯气和水反应生成盐酸和次氯酸,盐酸和足量碳酸钠反应生成氯化钠和碳酸氢钠,次氯酸和碳酸钠反应生成次氯酸钠和碳酸氢钠,所以方程式为Cl2+2Na2CO3+H2O=NaCl+NaClO+2NaHCO3,故答案为:Cl2+2Na2CO3+H2O=NaCl+NaClO+2NaHCO3.
(2)漂白粉的主要成分为CaCl2、Ca(ClO)2,Ca(ClO)2易与空气中二氧化碳和水反应生成HClO,HClO不稳定,见光分解生成HCl和水,最终生成CaCl2、CaCO3;
如漂白粉没有变质,则漂白粉中无CaCO3,加入盐酸后无气体放出且澄清石灰水未见浑浊;
如漂白粉全部变质,则产物为CaCl2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,则品红不褪色,而石灰水变浑浊;
如漂白粉部分变质,漂白粉中含有CaCl2、Ca(ClO)2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水变浑浊,
故答案为:CaCl2、CaCO3;
实验步骤预期现象和结论①再向B试管加入1mol/L的稀盐酸加入适量1mol/L的盐酸,塞上带导管的单孔塞,将导管的另一端插入A试管中若有气泡冒出,且澄清石灰水变浑浊则假设一步成立,假设二、三成立②用胶头滴管向上述步骤后的B试管中滴入几滴品红试液,振荡若品红溶液不褪色,则假设二成立,若品红溶液褪色,则假设三成立
本题解析:
本题难度:一般
2、选择题 近几年,液氯、液氨、硝基苯等物质的泄漏事故不断发生.下列说法正确的是( )
A.液氯能使干燥的红色布条褪色
B.液氨气化时吸收大量的热,可以用作致冷剂
C.工业上用苯的硝化生产硝基苯,其原料无毒,符合绿色化学理念
D.液氯、液氨、硝基苯泄漏都可以用NaOH溶液处理
参考答案:A.液氯不具有漂白性,不能使干燥的布条褪色,与水反应生成的HClO具有漂白性,故A错误;
B.氨易液化,液氨气化时吸收大量的热,可作制冷剂,故B正确;
C.工业生产硝基苯用苯和浓硝酸作原料,苯有毒,常用浓硫酸做催化剂,反应物不能完全转化为生成物,故C错误;
D.氯气和NaOH溶液反应,可用NaOH溶液处理,氨气水溶液呈碱性,应用酸处理,硝基苯用活性炭处理,故D错误.
故选B.
本题解析:
本题难度:简单
3、选择题 氯气跟下列物质反应时,能够产生白雾的是
[? ]
A.Na
B.Cu
C.H2
D.Fe
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列关于氯水的叙述中,正确的是:?
A.新制氯水中没有分子,只有离子
B.新制氯水在光照的条件下,可以产生气体,该气体是氯气
C.新制氯水中滴加硝酸银溶液,没有任何现象
D.氯气可以使湿润的有色布条褪色
参考答案:D
本题解析:考查氯水的成分及性质
A:氯水中存在水、次氯酸及氯气三种分子,错
B:Cl2+H2O=HCl+HClO? 2HClO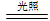 2HCl+O2↑,故该气体为氧气
2HCl+O2↑,故该气体为氧气
C:氯水中的氯离子可与银离子生成白色沉淀
D:氯水中的次氯酸具有强氧化性、漂白性,可使湿润的有色布条褪色
故答案为D
本题难度:简单
5、填空题 氯系消毒剂的作用原理:__________________________?
明矾净水原理(方程式)_____________________________??
漂白粉失效原理(方程式): ___________________________??
参考答案:

本题解析:略
本题难度:一般