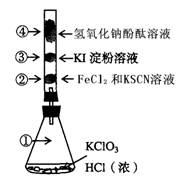
1������� (12��).��֪�������������Ũ���ᷴӦ�ų�������KClO3 + 6 HCl ="?" KCl + 3Cl2 ��+3H2O��ijУ��ѧ�С���ְ���ͼ����±�ص�����ʵ�顣��������װ�зֱ���в�ͬ��Һ����ɫ����Ӧһ��ʱ��۲����
��1������ͼ��ָ����λ��ɫ�仯Ϊ
��2��.д���������ӷ�Ӧ����ʽ_____________________________________.
д���������ӷ�Ӧ����ʽ____________________________________________
��3��.���KClO3 +? 6 HCl ="?" KCl + 3Cl2 ��+ 3 H2O��Ӧ�е���ת�Ƶķ������Ŀ.
2��ѡ���� ����������ͬʱ�����ȷ��ӣ�Cl2���������ӣ�Cl�D������?��?��
A��Һ��
B��������ˮ
C��CaCl2��Һ
D��������
3��ѡ���� ���¶�ʵ�鼰���������������ǣ�������
A��������ʹʪ�����ɫʯ����ֽ���
B�������������ͨ�뵽ʪ��ĺ첼���У��첼����ɫ
C����SO2��ˮ��Һ�е���Ʒ����Һ������Һ��ɫ�������Ⱥ���Һ�ֱ�ɺ�ɫ
D�����廯����Һ�е������Ƶ���ˮ����Һ�ʻ�ɫ
4��ѡ���� ���й���Cl2��SO2��˵����ȷ���ǣ�������
A������Ư��ԭ����ͬ
B�����߶�����ˮ���գ�������Ⱦ
C�����߶�������������ԭ��Ӧ
D�����߶����ж�����
5������� ���Ƶ���ˮ���еķ��Ӻ����ӣ��ֱַ�������ʵ�飺����ɫʯ����Һ���룬��Һ�Ժ�ɫ�������õ�������______��������Һ����ȥ�������õ�������______������AgNO3��Һ���в�����ϡ����İ�ɫ�������ɣ������õ�������______��