1、填空题 已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
(1)用太阳能分解5mol液态水消耗的能量是______kJ;
(2)液态甲醇不完全燃烧生成一氧化碳气体和液态水的热化学方程式为______;
(3)在以甲醇为燃料的燃料电池中,电解质溶液为酸性,则正极的电极反应式为______;?理想状态下,该燃料电池消耗2mol甲醇所能产生的最大电能为1162.4kJ,则该燃料电池的理论效率为______.(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)
2、填空题 依据事实,写出下列的热化学反应方程式:
1molN2(g)与适量H2(g)起反应,生成NH3(g),放出92.2kj热量。
_____________________________________________________________________。
3、选择题 已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
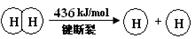
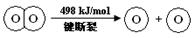
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H―O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H―H 键比 H2O(g) 中的H―O 键牢固

 O2(g)="==="
O2(g)="==="  P4O10(s) ΔH=-738.5 kJ・mol-1 ②
P4O10(s) ΔH=-738.5 kJ・mol-1 ②