1、选择题 草酸是二元弱酸,草酸氢钾溶液呈酸性.在0.1mol?L-1KHC2O4溶液中,下列关系正确的是( )
A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)=0.1?mol?L-1
C.c(C2O42-)<c(H2C2O4)
D.c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
参考答案:A.溶液遵循电中性原则,则有c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-),故A错误;
B.草酸氢钾溶液中存在H2C2O4、C2O42-、HC2O4-,根据物料守恒可知c(H2C2O4)+c(C2O42-)+c(HC2O4-)=0.1mol/L,故B错误;
C.草酸氢钾溶液呈酸性,说明HC2O4-电离程度大于水解程度,则c(C2O42-)>c(H2C2O4),故C错误;
D.在0.1mol?L-1KHC2O4溶液中,存在H2C2O4、C2O42-、HC2O4-和K+,根据物料守恒可知c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-),故D正确.
故选D.
本题解析:
本题难度:简单
2、选择题 (10分)写出下列物质在水中的电离方程式:
NaHSO4 HClO
Al(OH)3 Ca(OH)2
H2CO3
参考答案:NaHSO4=Na++H++SO42-; HClO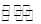 H++ClO-; Al(OH)3
H++ClO-; Al(OH)3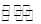 Al3++3OH-; Ca(OH)2=Ca2++2OH-; H2CO3
Al3++3OH-; Ca(OH)2=Ca2++2OH-; H2CO3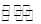 H++HCO3-; HCO3-
H++HCO3-; HCO3-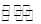 H++CO32-
H++CO32-
本题解析:
试题解析:硫酸氢钠是强电解质,能完全电离出钠离子、氢离子、硫酸根离子,电离方程式为:NaHSO4=Na++H++SO42-;HClO是弱电解质,不完全电离,电离方程式为:HClO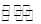 H++ClO-;氢氧化铝是弱碱,不完全电离,电离方程式为:Al(OH)3
H++ClO-;氢氧化铝是弱碱,不完全电离,电离方程式为:Al(OH)3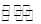 Al3++3OH-;Ca(OH)2是强电解质,能完全电离出钙离子、氢氧根离子,电离方程式为:Ca(OH)2=Ca2++2OH-; 碳酸是弱电解质,分步电离,电离方程式为:H2CO3
Al3++3OH-;Ca(OH)2是强电解质,能完全电离出钙离子、氢氧根离子,电离方程式为:Ca(OH)2=Ca2++2OH-; 碳酸是弱电解质,分步电离,电离方程式为:H2CO3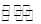 H++HCO3-;HCO3-
H++HCO3-;HCO3-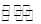 H++CO32-。
H++CO32-。
考点:电离方程式的书写
本题难度:一般
3、填空题 (12分)食醋分为酿造醋和配制醋两种。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)某研究小组利用滴定分析法测定某品牌食醋中醋酸的含量,下列说法正确的是?。
a.用NaOH溶液滴定时反应的离子方程式为:H++OH-=H2O
b.食醋试样需稀释一定倍数后再进行滴定
c.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
d.若测得该品牌食醋的物质的量浓度为0.75mol・L-1,则该食醋的总酸量为4.5g/100mL。
(2)研究小组的同学仔细观察了该品牌食醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与食品添加剂(苯甲酸钠C6H5COONa)不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的?(填选项字母)。
a.pH?b.电离度?c.电离常数?d.溶解度
(3)常温下,用0.1000 mol・L-1NaOH溶液分别滴定20.00mL 0.1000 mol・L-1HCl溶液和20.00mL 0.1000 mol・L-1CH3COOH溶液,得到2条滴定曲线,如下图所示。

图3?图4
①滴定醋酸溶液的曲线是?(填“图l”或“图2”);滴定曲线中a=?mL
(4)现欲粗略测定一未知浓度的CH3COOH溶液的电离度,应做的实验和所需的试剂(试纸)是?。
a.电解,NaOH溶液?b.蒸馏,Na2CO3溶液
c.酯化反应,石蕊试液? d.中和滴定,pH试纸图2
(5)酸式滴定管用蒸馏水润洗后,未用标准液润洗,导致滴定结果(填“偏小”、“偏大”或“无影响”)?;酸式滴定管读数时,若先俯后仰,则结果会?。
参考答案:(1)bd ?(2)c ?(3)①图2? 20.00mL?(4)d? (5)偏大?偏大
本题解析:(1)醋酸是弱酸,离子方程式中用化学式表示,a不正确。浓度过大,反应过快,不利于判断滴定终点,所以可以通过稀释来降低反应速率,b正确。醋酸和氢氧化钠反应,终点时溶液显碱性,因此选择酚酞作指示剂,不用甲基橙。物质的量浓度为0.75mol・L-1,则该食醋的总酸量为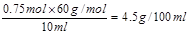 ,d正确。
,d正确。
(2)根据较强酸制取较弱的原理可判断,可通过比较二者的电离常数来比较其酸性强弱。
(3)盐酸和氢氧化钠恰好反应时溶液显中性,而醋酸和氢氧化钠恰好反应时溶液显碱性,所以图2表示醋酸的滴定曲线。
(4)电离度是指在一定温度下,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百分数。因此要测定醋酸的电离度,需要测定醋酸的物质的量浓度以及已电离的醋酸的物质的量浓度。根据电离方程式可知,可通过测定溶液的pH值来测定已电离的醋酸的物质的量浓度。
(5)酸式滴定管用蒸馏水润洗后,未用标准液润洗,则标准液被稀释,结果偏大。若先俯后仰,则消耗的体积偏大,结果会偏大。
本题难度:一般
4、选择题 有关常温下pH均为11的氨水和氢氧化钡溶液的说法正确的是( )
A.两种溶液中,由水电离出的氢氧根离子浓度均为1×10-11?mol?L-1
B.分别加水稀释100倍后,两种溶液的pH仍相同
C.氨水中的c(NH4+)和氢氧化钡中的c(Ba2+):后者是前者的两倍
D.用等浓度盐酸分别中和体积相等的两种溶液,消耗盐酸的体积相同
参考答案:A、两种溶液中,氢离子浓度为10-11mol/L,由水电离出的氢氧根离子浓度均为1×10-11?mol?L-1,故A正确;
B、氨水是弱碱存在电离平衡,稀释溶液促进弱电解质电离;分别加水稀释100倍后,氢氧化钡溶液是强碱的pH为9,氨水溶液是弱碱的pH小于9,故B错误;
C、氨水是弱碱存在电离平衡,PH相同氢氧根离子浓度相同,;氨水中的c(NH4+)和氢氧化钡中的c(Ba2+)相同,故C错误;
D、用等浓度盐酸分别中和体积相等的两种溶液,氨水是弱电解质,消耗盐酸的体积多,故D错误;
故选A.
本题解析:
本题难度:一般
5、选择题 下列事实能说明氨水是弱电解质的是
[? ]
A.氨水与氯化铝溶液反应产生氢氧化铝沉淀
B.用氨水做导电实验,灯泡很暗
C.0.1mol/L的氨水的pH<13
D.氯化铵溶液的pH<7
参考答案:CD
本题解析:
本题难度:简单