��2��
ʵ������
��Է���ʽ�٢ڻ��______
______
______��
��Է���ʽ��______
______��
��Һ��dz����ɫ��ɳȻ�ɫ
�йط�Ӧ�����ӷ���ʽ
��Al3++3OH-�TAl��OH��3��
��Al��OH��3+OH-�TAlO2-+H2O
���Al3++4OH-�TAlO2-+2H2O
��Mg2++2OH-�TMg��OH��2��
����
�����ԣ�Mg��Al
�ǽ����ԣ�
�ο��𰸣����ݷ���ʽ��Al3++3OH-�TAl��OH��3����Al��OH��3+OH-�TAlO2-+H2O���Al3++4OH-�TAlO2-+2H2O��֪���õ����Լ��У�AlCl3��Һ��MgCl2��Һ��NaOH��Һ�����������ȿ��Ժ�ǿ�ᷴӦ�����Ժ�ǿ�Ӧ�����������������������þֻ�ܺ�ǿ�ᷴӦ�����ڼ�����ԣ�������þ����������������֤������þ�Ļ�����ǿ�ڽ�������
������������ǿ���嵥�ʣ�������ǿ�Ŀ��Խ����������Ĵ������û������������������û��嵥�ʿ��Եó�Cl�ķǽ�����ǿ��Br��ԭ������ʽΪ��2Br-+Cl2�TBr2+2Cl-���õ����Լ��ǣ���ˮ��NaBr��Һ���ʴ�Ϊ��ʵ�鷽����ֻҪ����дѡ���Լ�����1����2��AlCl3��Һ��MgCl2��Һ��NaOH��Һ��ˮ��NaBr��Һʵ�������Թ��������ɰ�ɫ���������ɫ������ʧ��
�Թ����а�ɫ�������йط�Ӧ�����ӷ���ʽ2Br-+Cl2�TBr2+2Cl-���۷ǽ����ԣ�Cl��Br��
���������
�����Ѷȣ�һ��
3��ʵ���� ��16�֣�ijͬѧ��ͨ����ͼװ��ʵ�顢̽��SO2��Na2O2��Ӧ�IJ��
���г�װ������ȥ��װ�õ����������ã�
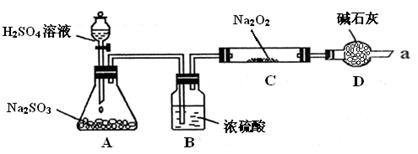
��װ��B������������ˮ������SO2���壬��ԭ���ǣ������ӷ���ʽ��ʾ��
?��
װ��D�������չ�����SO2��������Ⱦ�����⣬����������
?��
��ijͬѧ��ͨ����ͼʵ��װ�ã����鷴Ӧ���Ƿ���O2����ʱ����ʵ����������ǣ�
��?��?
�����ô����ǵ�ľ����������ܿ�a���۲����Ƿ�ȼ��
��C�й������������¼��裺
����1��ֻ��Na2SO3
����2��ֻ��Na2SO4
����3��?��
��1��������2������д����������Ӧ�Ļ�ѧ����ʽ
?��
��2����Na2O2��Ӧ��ȫ��Ϊȷ��C�й������ijɷ֣����������ʵ�飺

�ó����ۣ�������Na2SO4��
�÷����Ƿ����??����ǡ�����
��3�����ʵ����֤����3��ʵ�鲽�����£�
ʵ�鲽��
| ʵ������
| �ٵμ��������ϡ����
| �����ݼ�����ζ����
| �ڵμ���������BaCl2��Һ
| ������ɫ������
| ��ȡ����C�й���������Թ��У���������������ˮ�ܽ�
| ?
|
������3��������ȷ��ʵ�����˳����?
�ο��𰸣���16�֣�
��2Na2O2 + 2H2O = 4Na+ + 4OH- +O2����3�֣�
D����ֹ�����е�ˮ�����Ͷ�����̼����Cװ����Na2O2��Ӧ��2�֣�
��Һ©���Ͽ�ƿ�����¿���������2�֣�
����Na2SO3��Na2SO4��2�֣�?��1��Na2O2 + SO2 = Na2SO4 ��3�֣�
��2����2�֣�?��3���ۢ٢ڣ�2�֣�
�����������
�����Ѷȣ�һ��
4��ʵ���� ��13�֣����������еij���������Ҳ�Ǹ�����ѧ�Ĺ���Ԫ�أ�������ṹ�ص㣬�����仯���ʷ�Ӧʱ�������ֳ���ͬ�ļ�̬��ij�о���ѧϰС���������Ӧ���������Ļ��ϼ۽�����̽���������������ʵ�飬��ʵ��IJ���Ϊ��
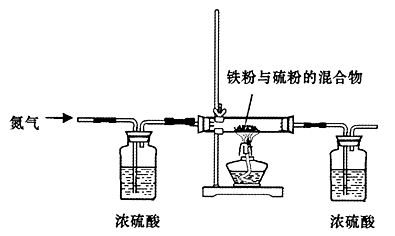
����һ�������ۺ���۰�һ�������Ȼ�ϣ���ͼ��ʾ�ڵ��������У����Ⱥ������ɷ������������У���ȴ��õ���ɫ���塣
�������ȡ��ɫ��������������ŨNaOH��Һ�����Լ��ȣ���ȴ����ˣ��õ���ɫ������
��ȡ�ú�ɫ������ͬѧ�Ǿ������۷���������ɷ�����˸��ֲ��룬���д����Ե�Ϊ��
����һ�������������ͬһ����Ԫ�أ����Ժ�ɫ����Ŀ�����Fe3S4
����������������ͬһ����Ԫ�أ�����ķǽ������������ɫ����ΪFeS
Ϊ����֤���ϲ����ֽ��������²�����
���������������м�������е�ϡ���ᡣ
�����ģ�ȡ������������Һ������������
��ش��������⣺
��1���������ϣ�ʵ���ҿ������Ȼ�隣�����Һ���������ƣ�NaNO2��������Һ��ϼ��ȷ�Ӧ�õ�������д���÷�Ӧ�����ӷ���ʽ��?��
��2��ʵ����ͨ�뵪��������?��
��3��������һ��ȷ��������Ӧ�ù۲쵽�Թ�����?���֣���ʵ������
��4�����������ȷ������ɲ����ĵ�ʵ�����������ͽ���?��
��5������һ�����ۺ���۵Ļ�Ϸ�ĩ����Ҫ����Щ����ԭ����?��
��6��������м���ŨNaOH��Һ�����Լ��ȵ�Ŀ����?��
�ο��𰸣�(1)NH4+ + NO2-  ?N2��+2H2O? (2��) ?N2��+2H2O? (2��)
(2)����װ���еĿ���? (2��)
(3)�а�ɫ���dz���? (2��)
(4)ȡ������������Һ�������μ�KSCN��Һ������Һ���Ժ�ɫ��������Һ�еμ�������ˮ����Һ�Ժ�ɫ��֤��ԭ��Һ��ֻ����Fe2+�����ɫ���������Ļ��ϼ�Ϊ+2�ۡ�(3��)
(5)��ֹδ��Ӧ������ϡ���ᷴӦ����Fe2+����ʵ��?(2��)
(6)��ȥδ��Ӧ����?(2��)
�����������1����Ԫ�ط����˹��з�Ӧ��NH4+ + NO2-  ?N2��+2H2O ?N2��+2H2O
��2����ֹ���ۻ���۱���������
��3��������Һ�������������������������ʣ�2Fe3����H2S=2Fe2����S����2H�����е���ɫ�����ɫ���dz���
��4��Ҳ�����������ӵļ��飨FeS��2H��=Fe2����H2S������
ȡ������������Һ�������μ�KSCN��Һ������Һ���Ժ�ɫ��������Һ�еμ�������ˮ����Һ�Ժ�ɫ��֤��ԭ��Һ��ֻ����Fe2+�����ɫ���������Ļ��ϼ�Ϊ+2��
��5���ڲ������й����м��ᣬ��Ҫͨ����Fe2+�ļ������ж�FeS�����������������Fe2+�����Ա���ʹ��۹���
��6��������������ڼ�Һ��3S��6OH��=S2����SO32����3H2O
�����Ѷȣ���
5������� (13 ��)��һ�������ĩ����CaCO3��Na2SO4��KCl��Ba (NO3)2��CuSO4�е�����������ɣ�ȡ��Ʒ��������ʵ�飺

��1��д��ʵ������з�����Ӧ�Ļ�ѧ����ʽ��?��
��2�������ĩ��һ�������ڵ�������?��һ�����ڵ�������?��
��3���������ĩ���ܵ���������±��������Բ�������Ҳ�����ٲ��䡣��
��4�������һ��ʵ���һ��ȷ����������ɣ�����ʵ�鲽�衢����ͽ��ۡ�
?
�ο��𰸣���1��CaCO3+2HCl=CaCl2+H2O+CO2����2�֣�
��2��CuSO4����2�֣�? CaCO3��KCl����2�֣�
��3������2�֣�
I
CaCO3��Na2SO4��KCl
II
CaCO3��KCl��Ba (NO3)2
�����������
�����Ѷȣ���
|