1、填空题 (8分)化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏 特列原理。请回答下列问题。
特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g) 4C(g)?
4C(g)?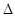 H >0?达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是?;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是?
H >0?达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是?;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是?
①增加C的物质的量?②加?压?③升 温?④使用催化剂
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化曲线的是?(填“A”或“B”)。设盐酸中加入的Zn质量为m1, 醋酸溶液中加入的Zn质量为m2。则m1?m2(选填“<”、“=”、“>”)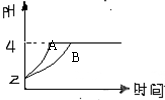
2、填空题 (10分)高炉炼铁中发生的基本反应之一:FeO(s)+CO(g) Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值?,平衡常数K值?(均选填“增大”“减小”或“不变”)。
(2)1 100 ℃时测得高炉中[CO2]="0.025" mol・L-1,[CO]="0.1" mol・L-1,在这种情况下,该反应是否处于化学平衡状态?(选填“是”或“否”),此时,化学反应速率v(正)??v(逆)(填“大于”“小于”或“等于”),其原因是?。
3、填空题 (10分)在一定条件下的下列可逆反应达到平衡时,试填出:xA+yB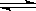 zC
zC
(1)若A、B、C都是气体,增大压强,平衡向正反应方向移动,则x+y与z关系是_____?__;
(2)若A、C是气体,且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向?方向移动;
(3)若B、C是气体,A是固体,增大A的浓度,平衡?(填“正向移动”、“逆向移动”或“不移动”);
(4)若升高温度后,C的百分含量减小,则正反应是?(填“吸热”或“放热”)反应。
(5)若该可逆反应达到平衡时加入催化剂,平衡?(填“正向移动”、“逆向移动”或“不移动”);
4、选择题 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图。下列叙述中正确的是

[? ]
A.?反应的化学方程式为5Y X
X
B.?t1时,Y的浓度是X浓度的1.5倍
C.?t2时,正、逆反应速率相等
D.?t3时,逆反应速率大于正反应速率
5、选择题 在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )
A.平衡向正反应方向移动
B.物质A的转化率减小
C.物质B的质量分数减少
D.化学计量数关系a>b