1、选择题 在一个不传热的固定容积的密闭容器中,可逆反应
mA(g)+nB(g) pC(g)+qD(g),当m、n、p、q为任意正整数时,该可逆反应一定达到平衡状态的标志是:①体系的压强不再发生变化②体系的温度不再发生变化③A的转化率不再改变④各组分的百分含量不再改变⑤反应速率vA:vB:vC:vD=m:n:p:q。其中正确的是(?)
pC(g)+qD(g),当m、n、p、q为任意正整数时,该可逆反应一定达到平衡状态的标志是:①体系的压强不再发生变化②体系的温度不再发生变化③A的转化率不再改变④各组分的百分含量不再改变⑤反应速率vA:vB:vC:vD=m:n:p:q。其中正确的是(?)
A.②③④
B.①③⑤
C.①④⑤
D.①②③④⑤
参考答案:A
本题解析:体系的压强与方程式的系数有关,①不确定,BCD错误。对于一个不传热的固定容积的密闭容器中的可逆反应,当体系的温度不再发生变化也就是说明反应达到了平衡状态。A的转化率不再改变、各组分的百分含量不再改变,说明浓度不再改变。速率符合方程式的比值,不是平衡状态。
本题难度:简单
2、填空题 (10分)已知:合成氨反应为N2+3H2 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系?(填“I”“II”“III”)
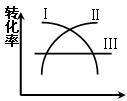
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为??(填“A”“B”“C”“D”)
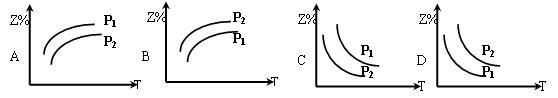
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ?;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) = ?
参考答案:(1)II(2分)(2)C(2分)(3)1:1(2分)(4)33.3%(2分)1:3:1(2分)
本题解析:略
本题难度:简单
3、选择题 往一真空密闭容器中通入一定量的气体A,在一定温度下,发生如下反应:
2A(g)?B(g)+xC(g)反应达平衡时,测得容器内压强增大了p%,若此时A的转化率为a%,下列关系正确的是
①若x=1,则p>a?②若x=2,则p<a?③若x=3,则p=a?④若x=4,则p≥a( )
A.②③
B.①④
C.②③④
D.②④
参考答案:设开始时加入气体A的物质的量为1 mol,则由题意得?
? 2A(g)=B(g)+xC(g)?
起始量(mol):1? 0? 0
变化量(mol):a%?12?a%? x2?a%?
平衡量(mol):1-a%?12a%? x2?a%
?总:1-12a%+x2?a%
?由题意知:1-12a%+x2?a%=1+p%,解得,ax=a+2p
代入①②③④选项分析判断,
①若x=1,则p>a? ?ax=a+2p? p=0,压强不变,故①错误;
②若x=2,则p<a? p=0.5a? 则p<a,故②正确;
③若x=3,则p=a? ?p=a? ③故正确;
④若x=4,则p≥a? p=1.5a? 则p>a,故④错误;
综上所述:②③正确;
故选A.
本题解析:
本题难度:简单
4、选择题 恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g)  N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是 (? )
N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是 (? )
A.若体积减小一半,则压强为原来的两倍
B.若体积减小一半,压强增大,但小于原来的两倍
C.平衡向右移动,混合气体颜色一定会变浅
D.平衡向右移动,混合气体密度减小
参考答案:B
本题解析:慢慢压缩气体体积到原来的一半,如果平衡不动,则压强为原来的两倍,但是平衡要正向移动,压强小于原来的两倍,所以A错、B正确。虽然平衡正向移动,但是NO2的浓度比原平衡大,所以颜色加深,C错,压缩前后气体的质量不变,体积缩小,密度增大,D错。答案选B。
点评:改变影响平衡移动的一个因素,平衡总是向减弱这种改变的方向移动。
本题难度:一般
5、选择题 在一密闭容器中,反应mA(g)+nB(g) pC(g),达到平时,测得c(A)为0.5 mol・L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol・L-1。则下列判断正确的是
pC(g),达到平时,测得c(A)为0.5 mol・L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol・L-1。则下列判断正确的是
A.化学计量数:m + n < p? B.平衡向逆反应方向移动了
C.物质B的转化率减小了? D.物质C的质量分数增加了
参考答案:BC
本题解析:略
本题难度:一般