1、选择题 下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
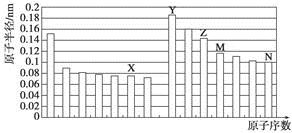
A.Z、N两种元素的离子半径相比,前者较大
B.X、N两种元素的气态氢化物的沸点相比,前者较低
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
参考答案:D
本题解析:根据原子半径的递变规律,X为O,Y为Na,Z为Al,M为Si,N为Cl。A项,离子半径:Cl->Al3+;B项,沸点:H2O>HCl;C项,SiO2既能与HF反应,也能与NaOH溶液反应,错误;D项,Al2O3是两性氧化物,既可以和NaOH(Y)溶液反应,又能与HCl(N)反应。
本题难度:一般
2、选择题 短周期元素X、Y、Z、W 的原子序数依次增大,X原子的最外层电子数是内层电子数的2倍,X与Z同主族,Y和氢元素同主族,W原子的最外层电子数比次外层电子数少1。下列说法正确的是
A.元素X形成的单质一定是原子晶体
B.原子半径的大小顺序:r(W)>r(Z)>r(Y) >r (X)
C.Y与氧元素形成的化合物Y2O2中阴、阳离子的个数比为1:2
D.W分别与Y、Z形成的化合物中含有的化学键类型相同
参考答案:C
本题解析:X原子的最外层电子数是内层电子数的2倍,x为碳;X与Z同主族,Z为硅;Y和氢元素同主族,为钠;W原子的最外层电子数比次外层电子数少1,为氯。A.元素X形成的单质有金刚石,C60分子,前者是原子晶体,后者是分子晶体,错误;B原子半径的大小顺序:Na>Si>Cl>C ,错误;C.Y与氧元素形成的化合物是过氧化钠,Na2O2中阴O22-、阳离子Na+的个数比为1:2,正确。D.W分别与Y、Z形成的化合物是氯化钠和四氯化硅,前者是离子键,后者是共价键,所含有的化学键类型不相同,错误;
本题难度:一般
3、选择题 已知X、Y、Z和R分别代表4种元素。如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的原子序数),则下列关系正确的是( )
A.a-c=m-n
B.a-b=n-m
C.c-d=m+n
D.b-d=n+m
参考答案:D
本题解析:由题意可知,四离子的核外电子数相同,即:a-m=b-n=c+n=d+m,进而可得出只有D项正确。
本题难度:一般
4、简答题 【选修3-物质的结构与性质】(15分)

上表为周期表的一部分,其中的编号代表所对应的元素。请回答下列问题:
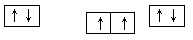
(1)⑨号元素的基态原子的价电子排布式是________,与其同周期,且基态原子的核外未成对电子数最多的元素是______(写出元素符号),②号元素基态原子的电子排布图为___。
(2) ①号与③号元素形成的含有18电子的物质为________(写出名称),②号与③号元素形成的,能造成温室效应的物质的空间构型为________。
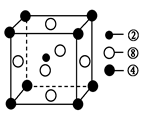
②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为________(用对应的元素符号表示),常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因是____________。
(3)①、②两种元素能形成多种平面形分子,其中有一种相对分子质量最小,有关该分子的说法中正确的是________。
a.该分子属于含有极性键的非极性分子b.该分子含有4个σ键和1个π键
c.该分子中的②原子采取sp2杂化d.该物质易溶于水,并能和水反应得到酒精
(4)某元素的价电子排布式为nsnnpn+1,该元素可与元素①形成含有10个电子的分子X,将过量的X通入盛有硫酸铜溶液的试管里,产生的现象为_______。
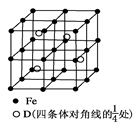
(5) 若D元素与Fe元素形成某种晶体如图所示。若晶胞的边长为a nm,则合金的密度为________g/cm3。
参考答案:(1) 3d104s1 (1分)?Cr (1分) ?
 ?
?
(1分)
(2)?过氧化氢? (1分)?直线型 (1分)? MgNi3C或Ni3MgC? (2分)?
甲醇分子间存在氢键,而丙烯分子间只有范德华力? (2分)
(3)ac? (2分)
(4)先产生蓝色沉淀,后沉淀消失,溶液变成深蓝色? (2分)
(5 )? 0.92/a3或5.56×1023/(a3NA)? (2分)
本题解析:(1)⑨号元素为铜元素,基态原子的价电子排布式是3d104s1,与其同周期,且基态原子的核外未成对电子数最多的元素的电子排布式为[Ar]3d54s1是Cr,②号元素为碳元素,基态原子的电子排布图?

(2) ①号元素氢与③号元素氧形成的含有18电子的物质为过氧化氢,②号元素碳与③号元?素氧形成的,能造成温室效应的物质二氧化碳的空间构型为直线型。根据晶胞的结构利用切割法判断,1个晶胞中含有1个碳原子,镁原子8×1/8=1个,镍原子6×1/2=3个,C、Mg、Ni三种元素的原子形成的晶体的化学式为MgNi3C或Ni3MgC,常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因是甲醇分子间存在氢键,而丙烯分子间只有范德华力。
(3)C、H两种元素能形成多种平面形分子,其中有一种相对分子质量最小为?乙炔,a.该分子中碳氢键为极性键,分子结构对称,属于含有极性键的非极性分子,正确;b.该分子含有2个碳氢键和1个碳碳三键,共3个σ键和2个π键,错误;c.该分子为直线型,碳原子采取sp1杂化,错误;d、该物质微溶于水,错误,选a;
(4)某元素的价电子排布式为nsnnpn+1,该元素为氮元素,可与元素氢形成含有10个电子的分子氨气,将过量的氨气通入盛有硫酸铜溶液的试管里,先发生复分解反应后发生络合反应,产生的现象为先产生蓝色沉淀,后沉淀消失,溶液变成深蓝色。
(5) 根据晶胞的结构先确定1个晶胞中含有各原子的个数,进一步确定化学式,结合密度的定义及相关数学知识进行计算。无法确定D元素,无法计算
本题难度:一般
5、选择题 下列不是元素电负性应用的是(?)
A.判断一种元素是金属还是非金属
B.判断化合物中元素的化合价
C.判断化学键类型
D.判断化合物的溶解度
参考答案:D
本题解析:电负性是用来描述不同元素的原子对键合电子吸引力的大小,所以物质的溶解度和电负性大小无关,其余都是与电负性有关系的,答案选D。
本题难度:一般