1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4==Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
[? ]
? 反应温度/℃? Na2S2O3溶液? 稀H2SO4? H2O
? ? V/mL?c/(mol・L-1)? V/mL?c/(mol・L-1)? V/mL?
A? 25? ?5? 0.1? 10?0.1? 5
B?25? 5?0.2? 5?0.2? 10
C? 35? ?5? ?0.1?10? 0.1? 5
D? 35? 5?0.2? 5? 0.2? 10
参考答案:D
本题解析:
本题难度:一般
2、选择题 右图曲线a表示放热反应? X(g) + Y(g)  ?Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
?Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是

A.升高温度
B.加大X的投入量
C.加催化剂
D.增大体积
参考答案:C
本题解析:由图象可知,由曲线a到曲线b,到达平衡的时间缩短,改变条件,反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,该反应正反应是放热反应,升高温度,反应速率加快,平衡向逆反应移动,x的转化率降低,故A错误;加大X的投入量,X浓度增大,反应速率加快,平衡向正反应移动,但x的转化率降低,故B错误;加入催化剂,反应速率加快,催化剂不影响平衡移动,x的转化率不变,故C正确;增大体积,压强减小,该反应前后气体的物质的量不变,压强降低平衡不移动,但反应速率降低,故D错误,所以本题的答案选择C。
点评:本题考查了平衡的移动,该考点是高考考查的重点,本题要抓住的是X的转化率不变且达到平衡的时间缩短,例如若选项中如果增大压强也可以选择,该题难度中等。
本题难度:一般
3、填空题 反应A+3B=2C+2D.在四种不同的情况下的反应速率分别为:
①υ(A)=0.15mol/(L-s)?②υ(B)=0.6mol/(L-s)
③υ(C)=0.4mol/(L-s)?④υ(D)=0.45mol/(L-s)
该反应进行的快慢顺序为(用序号表示)______.
参考答案:在同一反应中,化学反应速率之比等于其计量数之比,把所有物质的反应速率换算成A的反应速率.?
? ①υ(A)=0.15mol/(L?s)?
②由υ(B)=0.6 mol/(L?s)知,υ(A)=0.2mol/(L?s)
③由υ(C)=0.4mol/(L?s)知,υ(A)=0.2mol/(L?s)
④由υ(D)=0.45mol/(L?s)知,υ(A)=0.225mol/(L?s)
故答案为:④>②=③>①.
本题解析:
本题难度:一般
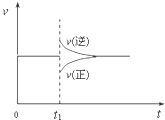
4、选择题 在一定条件下,向一带活塞的密闭容器中充入2mol?NO2,发生下列反应2NO2(g)?N2O4(g)△H<0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图.下列对t1时刻改变条件的推测中正确的是( )
A.保持压强不变,升高反应温度
B.保持温度和容器体积不变,充入1mol?N2(g)
C.保持温度和容器体积不变,充入1mol?N2O4?(g)
D.保持温度和压强不变,充入1mol?N2O4?(g)