1、填空题 (16分)
(1)已知298K时,Fe(OH)3的溶度积常数 =2.6×10-39,Mg(OH)2的溶度积常数
=2.6×10-39,Mg(OH)2的溶度积常数 =5.6×
=5.6× ,取适量浓度均为0.1mol/L的MgCl2和FeCl3混合液(含HCl),加入一定量的MgCO3达到沉淀溶液平衡,测得pH=4.00,则此温度下残留在溶液中的c(Fe3+)=______________;
,取适量浓度均为0.1mol/L的MgCl2和FeCl3混合液(含HCl),加入一定量的MgCO3达到沉淀溶液平衡,测得pH=4.00,则此温度下残留在溶液中的c(Fe3+)=______________;
有没有Mg(OH)2沉淀生成______________填“有”或“无”),理由是________________________________。
(2)酸HnA与碱B(OH)m完全反应生成正盐.
①若HnA为HCl,且该盐溶液的pH<7,用离子方程式说明原因:
②若将0.4mol・L-1的NaOH溶液与0.2mol・L-1的HnA溶液等体积混合后pH=10,
则HnA为 (填序号).
a.一元强酸 b. 一元弱酸 c. 二元强酸 d. 二元弱酸
(3)某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:回答下列问题:

2、选择题 在25℃时,用蒸馏水稀释1 mol/L的醋酸溶液至0.01 mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是? ( )
A.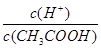
B.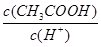
C.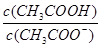
D.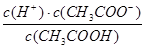
3、选择题 室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
[? ]
A.加水稀释2倍后,两溶液的pH均减小
B.使温度都升高20℃后,两溶液的pH均不变
C.加适量的醋酸钠晶体后,两溶液的pH均增大
D.加足量的锌充分反应后,醋酸产生的氢气比盐酸多
4、选择题 常温下,0.1mol?L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是( )
A.该溶液中水电离出的c(H+)=1×10-10mol?L-1
B.该溶液中c(H+)+c(A-)+c(HA)=0.1mol?L-1
C.该溶液与0.05mol?L-1NaOH溶液等体积混合后:c(A-)>c(Na+)>c(OH-)>c(H+)
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
5、简答题 Ⅰ.已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数分别为:
| ① | HF | Ka=6.8×10-4mol?L-1
②
CH3COOH
Ka=1.7×10-5mol?L-1
③
HCN
Ka=6.2×10-10mol?L-1
④
H2CO3
Ka1=4.4×10-7mol?L-1
Ka2=4.7×10-11mol?L-1
|
根据上述数据,回答下列问题:
(1)四种酸中酸性最强的是______,四种酸中酸性最弱的是______.
(2)写出H2CO3电离方程式是______、______.
(3)写出下列反应的化学方程式:足量的氢氟酸与碳酸钠溶液混合:______;足量的CO2通入NaCN溶液中:______.
Ⅱ.氨水中存在:NH3?H2O?NH4++OH-,在5份0.01mol?L-1的氨水中分别加入下列各物质:
A.浓氨水B.纯水C.少量NaOH固体D.少量浓硫酸 E.NH4Cl固体
按照要求填空:
(1)电离平衡会向正向移动是______;电离平衡会向逆向移动是______.
(2)c(NH4+)、c(OH-)都增大的是______;c(NH4+)、c(OH-)都较小的是______.
(3)c(NH4+)增大,c(OH-)减小的是______;c(NH4+)减小,c(OH-)增大的是______.