1������� ��16�֣�
��1����֪298Kʱ��Fe(OH)3���ܶȻ����� =2.6��10-39��Mg(OH)2���ܶȻ�����
=2.6��10-39��Mg(OH)2���ܶȻ����� =5.6��
=5.6�� ��ȡ����Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��FeCl3���Һ����HCl��������һ������MgCO3�ﵽ������Һƽ�⣬���pH=4.00������¶��²�������Һ�е�c(Fe3+)=______________��
��ȡ����Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��FeCl3���Һ����HCl��������һ������MgCO3�ﵽ������Һƽ�⣬���pH=4.00������¶��²�������Һ�е�c(Fe3+)=______________��
��û��Mg(OH)2��������______________��С����ޡ�����������________________________________��
��2����HnA���B(OH)m��ȫ��Ӧ��������.
����HnAΪHCl���Ҹ�����Һ��pH��7�������ӷ���ʽ˵��ԭ��
������0.4mol��L��1��NaOH��Һ��0.2mol��L��1��HnA��Һ�������Ϻ�pH=10��
��HnAΪ ������ţ�.
a.һԪǿ�� b. һԪ���� c. ��Ԫǿ�� d. ��Ԫ����
��3��ijѧУ������ȤС��Ӻ�ˮɹ�κ����±(��Ҫ��Na+��Mg2+��Cl����Br����)��ģ�ҵ��������ȡþ����Ҫ�������£��ش��������⣺

�ο��𰸣�
���������
�����Ѷȣ�һ��
2��ѡ���� ��25��ʱ��������ˮϡ��1 mol/L�Ĵ�����Һ��0.01 mol/L������Һ��ϡ�ͣ����и�����ʼ�ձ����������Ƶ���? (����)
A��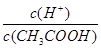
B��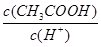
C��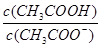
D��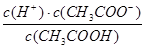
�ο��𰸣�A
���������������������ʣ���ˮϡ�ʹ��ᣬ�ٽ�������룬��n��CH3COO������n��H��������n��CH3COOH����С������������ӡ�������Ũ������ij̶�С����Һ�������ij̶ȣ�����c��CH3COO������c��H������c��CH3COOH������С����c(OH��)���ݴ˷������
A�м�ˮϡ�ʹ��ᣬ�ٽ�������룬n��H+������n��CH3COOH����С������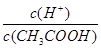 ������ȷ��
������ȷ��
B�м�ˮϡ�ʹ��ᣬ�ٽ�������룬n��H+������n��CH3COOH����С������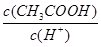 ��С��B����ȷ��
��С��B����ȷ��
C�м�ˮϡ�ʹ��ᣬ�ٽ�������룬n��CH3COOH����С��n��CH3COO����������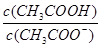 ��С��C����ȷ��
��С��C����ȷ��
D���¶Ȳ��䣬����ĵ���ƽ�ⳣ�����䣬��D����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ӱ��������ǿ������������ѧ������˼ά�����ͳ���˼ά������ע�����ƽ�ⳣ��ֻ���¶��йأ�����Һ��Ũ���أ�DΪ�״���
�����Ѷȣ�һ��
3��ѡ���� �����£�pH��ͬ�����ͬ�Ĵ��������������Һ�ֱ��ȡ���д�ʩ���й�������ȷ����
[? ]
A����ˮϡ��2��������Һ��pH����С
B��ʹ�¶ȶ�����20�������Һ��pH������
C���������Ĵ����ƾ��������Һ��pH������
D����������п��ַ�Ӧ��������������������
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
4��ѡ���� �����£�0.1mol?L-1ijһԪ�ᣨHA����Һ��c��OH-��/c��H+��=1��10-8������������ȷ���ǣ�������
A������Һ��ˮ�������c��H+��=1��10-10mol?L-1
B������Һ��c��H+��+c��A-��+c��HA��=0.1mol?L-1
C������Һ��0.05mol?L-1NaOH��Һ�������Ϻ�c��A-����c��Na+����c��OH-����c��H+��
D�������Һ�м���һ����NaA������ˮϡ�ͣ���Һ��c��OH-��������
�ο��𰸣�A����Һ��c��OH-��/c��H+��=1��10-8��Kw=C��H+��?C��OH-��=1��10-14����ʽ�е�������Ũ������Һ���������ģ�����������Ũ����ˮ������ģ��������C��H+��=0.001mol/L��ȷ��Ϊ������Һ��������Һ��C��OH-��=10-11mol/L����ˮ�������������Ũ��Ϊ10-11mol/L����A����
B��0.1mol?L-1ijһԪ�ᣨHA����Һ�д��ڵ���ƽ�⣬���Ը��������غ��֪c��A-��+c��HA��=0.1mol?L-1������c��H+��+c��A-��+c��HA��=0.1mol?L-1�Ǵ���ģ���B����
C��0.1mol?L-1ijһԪ�ᣨHA����Һ��0.05mol?L-1NaOH��Һ�������Ϻ�Ӧ����Ӧ�����ҺΪ��Ũ�ȵ���HA����NaA�Ļ��Һ����Һ��һ�����ڵ���غ㣻[H+]+[Na+]=[OH-]+[A-]������ѡ���е�����Ũ�ȴ�С����c��A-����c��Na+�������ݵ���غ�Ӧ��c��OH-����c��H+������C����
D��ͨ�������֪��Ϊ������� ����ƽ��HA?H++A-����ˮϡ�ʹٽ����룬������Ũ�ȼ�С������һ����NaA���壬�ܽ����ɵ�A-������������ĵ��룬������Ũ�ȼ�С�������¶�һ��ʱ��Һ��������Ũ��������������Ũ�ȳ˻�Ϊ����������ˮ�ͼ���һ����NaA���壬ʹ������Ũ�ȼ�С������������Ũ������D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
5������� ����֪����ᡢ���ᡢ�����ᣨHCN����̼���������µĵ��볣���ֱ�Ϊ��
| �� | HF | Ka=6.8��10-4mol?L-1
��
CH3COOH
Ka=1.7��10-5mol?L-1
��
HCN
Ka=6.2��10-10mol?L-1
��
H2CO3
Ka1=4.4��10-7mol?L-1
Ka2=4.7��10-11mol?L-1
|
�����������ݣ��ش��������⣺
��1����������������ǿ����______����������������������______��
��2��д��H2CO3���뷽��ʽ��______��______��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ���������������̼������Һ��ϣ�______��������CO2ͨ��NaCN��Һ�У�______��
��ˮ�д��ڣ�NH3?H2O?NH4++OH-����5��0.01mol?L-1�İ�ˮ�зֱ�������и����ʣ�
A��Ũ��ˮB����ˮC������NaOH����D������Ũ���� E��NH4Cl����
����Ҫ����գ�
��1������ƽ����������ƶ���______������ƽ����������ƶ���______��
��2��c��NH4+����c��OH-�����������______��c��NH4+����c��OH-����������______��
��3��c��NH4+������c��OH-��������______��c��NH4+������c��OH-���������______��
�ο��𰸣���1����������HF�ĵ���ƽ�ⳣ�������HF����ǿ��HCN�ĵ���ƽ�ⳣ����С����HCN����������
�ʴ�Ϊ��HF��HCN��
��2��̼��Ϊ��Ԫ���ᣬ�ֲ����룬�Ե�һ������Ϊ�������뷽��ʽΪH2CO3?HCO3-+H+��HCO3-?CO32-+H+��
�ʴ�Ϊ��H2CO3?HCO3-+H+��HCO3-?CO32-+H+��
��3������ǿ��HF��H2CO3��HCN��HCO3-���ɷ�����Ӧ����NaF��CO2����Ӧ�ķ���ʽΪ2HF+Na2CO3�T2NaF+H2O+CO2����������CO2ͨ��NaCN��Һ�У������ķ�Ӧ����ʽΪNaCN+H2O+CO2�THCN+NaHCO3��
�ʴ�Ϊ��2HF+Na2CO3�T2NaF+H2O+CO2����NaCN+H2O+CO2�THCN+NaHCO3��
��1����ˮϡ�ʹٽ�һˮ�ϰ����룬����Ũ��ˮ��һˮ�ϰ�Ũ������ƽ�������ƶ�������Ũ���ᣬ�����������ӷ�Ӧ�ٽ�һˮ�ϰ����룬���Դٽ�һˮ�ϰ��������ABD��
���������������ƣ�c��OH-����������һˮ�ϰ����룬���������Ȼ�泥�c��NH4+����������һˮ�ϰ����룬��������һˮ�ϰ��������CE��
�ʴ�Ϊ��ABD��CE��
��2������Һ�м���Ũ��ˮ���ٽ�һˮ�ϰ����룬��Һ��c��NH4+����c��OH-��������
����Һ�м���ˮ���ٽ�һˮ�ϰ����룬��笠����ӻ���������������ı���С����Һ�������ı���������c��NH4+����c��OH-������С��
�ʴ�Ϊ��A��B��
��3������Һ�м����Ȼ�泥�笠�����Ũ����������һˮ�ϰ����룬������������Ũ�ȼ�С������Һ�м����������ƹ��壬��Һ������������Ũ����������һˮ�ϰ����룬��笠�����Ũ�ȼ�С��
�ʴ�Ϊ��E��C��
���������
�����Ѷȣ���