1��ѡ���� ���³�ѹ�¹������ƿ���CO2��Ӧ����CO����Ӧ���ֽ�CO2��CO�Ļ��������һ�������º������������Ƴ�ַ�Ӧ������������������28 g������˵����ȷ����
A����Ӧ�����У�����ת����Ϊ2NA
B�����������������Ϊ106 g
C��CO������ʣ��
D����Ӧ��һ������11.2 L����
2������� ��1����-50��ʱ��Һ���������µ��룺2NH3?NH4++NH-2��k=2��10-12��Һ���ĵ���ﵽƽ��ʱ��������Ũ�ȴ�С��ϵΪ______������NH4Cl���壬K______2��10-12�����������������=����
��2����֪25��ʱKsp��AgCl��=1.8��10--10����10mL?0.10mol/L?AgNO3��Һ�м���10mL0.20mol/LNaCl��Һ����ַ�Ӧ����Һ�е�c��Ag+��=______��
��3����ƽ����������ǿ���Ʊ����������������ֳ���������Ļ�ѧ����ʽ��
______FeSO4
______Fe2O3+____________+____________
��4����֪����������ˮ����Һ�����ԣ���ͼ��ʾ������ʵ��װ���У���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.02mol���ӣ����������ε�ˮ�����Һ����ı仯����������������ȷ����______
A�����������������٣���
B����Һ��pH�仯���ټ�С��������
C���缫���������ʵ��������٣���
D���缫��Ӧʽ����������?2Cl--2e-?Cl2��? ���и���?2H++2e-?H2��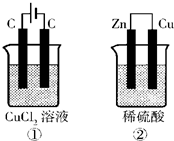
3��ѡ���� ��8NH3��3Cl2��N2��6NH4Cl��Ӧ�У�����21��3g Cl2�μӷ�Ӧ����������NH3������Ϊ?��?��
A��13��6g
B��10��2g
C��6��8g
D��3��4g
4��ѡ���� ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ��3Fe2����2S2O ?��O2��xOH��===Fe3O4��S4O
?��O2��xOH��===Fe3O4��S4O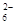 ?��2H2O������˵���У���ȷ����(����)
?��2H2O������˵���У���ȷ����(����)
A��ÿ����1mol Fe3O4����Ӧת�Ƶĵ�������Ϊ3mol
B��Fe2����S2O ���ǻ�ԭ��
���ǻ�ԭ��
C��1mol Fe2��������ʱ����Fe2����ԭ��O2�����ʵ���Ϊ1/3mol
D��x��2
5��ѡ���� ��ҵ��ұ�����л�ѧ����ʽ���£�Fe2O3+3CO 2Fe+3CO2�������������ԭ��Ӧ�У��������ͻ�ԭ�������ʵ���֮��Ϊ(? )
2Fe+3CO2�������������ԭ��Ӧ�У��������ͻ�ԭ�������ʵ���֮��Ϊ(? )
A��3�U1
B��2�U3
C��1�U3
D��3�U5