1、选择题 在一定温度下的定容密闭容器中,当下列条件不再改变时,表明反应:
A(s)+2B(g) C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是
A.混合气体的压强
B.混合气体的密度
C.气体的总物质的量
D.单位时间内生成n mol C的同时消耗2n molB
参考答案:B
本题解析:由反应方程式可以看出,反应前后气体体积不变,但气体的质量发生了改变。因此,当达到化学平衡时,气体的质量应保持不变,混合气体的密度也应保持不变。故答案选B。
点评:化学平衡移动的考查,是历年高考的重点,应特别注意有气体参与的反应。若反应前后气体体积发生变化,则可根据压强、混合气体的密度判断化学平衡。
本题难度:一般
2、选择题 在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生可逆反应3X(g)+Y(g) 2Z(g),并达到平衡。已知正反应是放热反应,测得X的转化率为37.5%,Y的转化率为25%,下列有关叙述正确的是(?)
2Z(g),并达到平衡。已知正反应是放热反应,测得X的转化率为37.5%,Y的转化率为25%,下列有关叙述正确的是(?)
A.若X的反应速率为0.2 mol・L-1・s-1,则Z的反应速率为0.3 mol・L-1・s-1
B.若向容器中充入氦气,压强增大,Y的转化率提高
C.升高温度,正反应速率减小,平衡向逆反应方向移动
D.开始充入容器中的X、Y物质的量之比为2∶1
参考答案:D
本题解析:A项错,X消耗速率为0.3 mol・(L・s)-1,转化为X和Y的Z的速率为0.2 mol・(L・s)-1才是平衡的标志。B项错,在容器容积不变时加入氦气,平衡不移动。C项错,升温时,正、逆反应速率均增大,但增幅不同。D项正确,设开始时充入X的物质的量为x,Y的物质的量为y,则x・37.5%∶y・25%=3∶1得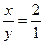 。
。
本题难度:一般
3、计算题 在5L密闭容器中,通入5 mol N2和8 mol H2,在一定条件下生成NH3,反应进行到2 min时,测得容器内有4 mol NH3。求:
(1)2min内的平均速率v(H2),v(N2),v(NH3)。
(2)2 min时,N2,H2的浓度。
参考答案:(l)v(H2)=0.2 mol/(L・min);v(N2) = 0. 6 mol/(L・min);v(NH3) = 0. 4 mol/(L・min)
(2)c(N2) = 0. 6 mol/L;c(H2) = 0. 4 mol/L
本题解析:
本题难度:一般
4、选择题 T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C物质的量变化如图(Ⅰ)所示;若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
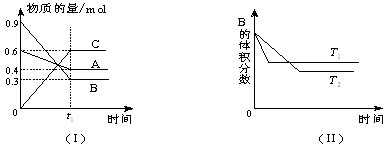
A.在(t1+1)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.在(t1+1)min时,保持容器压强不变,通入稀有气体,平衡向正反应方向移动
C.不再增减物质,只改变压强或温度时,A的体积分数V(A)%变化范围为25%<V(A)%<40%
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
参考答案:C
本题解析:由(I)图三物质的物质的量的变化值得可求得该可逆反应的化学方程式为:A+3B 3C;
3C;
可看出,加压,平衡正向移动,排除A;保持容器压强不变,通入稀有气体,相当于减压,平衡左移,排除B;
由(II)图可知,T1温度下先达到平衡,即T1>T2,并且温度越高,B的体积分数越大,说明升温平衡左移,A的转化率降低,排除D
在t1时刻反应达到平衡、采用极值法平衡向两方移动时各物质的量分别为:
化学反应:? A? +? 3B ? 3C
? 3C
t1时刻:? 0.4? 0.3? 0.6
完全正向移动:0.3? 0? 0.9?此时A的体积分数V(A)%=25%
完全逆向移动:0.6? 0.9? 0?此时A的体积分数V(A)%=40%
故答案为C
本题难度:一般
5、填空题 已知2SO2(g)+O2(g)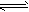 2SO3(g) △H=-196kJ・mol-1, 500℃时将2mol SO2和1molO2装入一体积恒定的
2SO3(g) △H=-196kJ・mol-1, 500℃时将2mol SO2和1molO2装入一体积恒定的
10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:
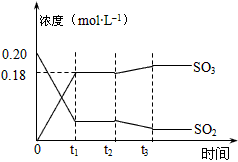
请回答下列问题
(1)用O2表示2分钟内该反应的平均反应速率为________mol・L-1・min-1。计算500℃时该反应的平衡常数
K=________,
(2)上图表示该反应在时刻t1达到平衡后,求平衡时O2的转化率________,时刻t2因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件可能是________________(写一个即可)。
(3)在上述条件下起始装入的SO2和O2各2mol,达平衡后设SO3的转化率为x,列出求x的方程
________________。(不必求出x)
(4)某温度时,该反应的平衡常数K=800,则该温度________500℃(填“>”、“<”、“=”)。
参考答案:(1)0.045;8100
(2)90%;增加O2浓度(或:降温)
(3)10x2/[(1-x)2(2-x)]=8100
(4)<
本题解析:
本题难度:一般