1��ѡ���� ���ʵ���֮��Ϊ2��5��п��ϡ����ǡ�÷�Ӧ�������ᱻ��ԭ�IJ���ΪN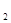 O����÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮���ǣ�?��
O����÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮���ǣ�?��
A��1:4
B��1:5
C��2:3
D��2:5
�ο��𰸣�A
�����������п�����ʵ�����2x����ϡ��������ʵ�����5x����������п��2x�������ԭ���غ��֪������ԭ��������5x��2x��2��x����÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮����x:4x��1:4����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣��Ҫ�ǿ���ѧ��������õ��ӵ�ʧ�غ�����й�������ԭ��Ӧ���������������������ѧ����������������
�����Ѷȣ�һ��
2��ѡ���� ���Ӿ�������Ĵ�����������NH4NO3��Zn�۰�������16:13��Ϸ������ȵ�ʯ�����ϣ�ʹ��ʱ��ˮ���β����ġ���֪������Ӧ����N2��ˮ���ɡ��йص�˵������ȷ���Ǣ�ˮ�����ܽ�NH4NO3���������������Լ�������Ӧ���������ã���1molNO3-�ڷ�Ӧ�е�5mol e-���۳�������������пС��������NH4+��������
A���٢�
B���ڢ�
C���ۢ�
D���٢�
�ο��𰸣�B
�����������NH4NO3��Zn�۰�������8��6��5��Ϸ������ȵ�ʯ�����ϣ��������ʵ���֮��=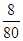 ��
��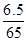 =1��1��ʹ��ʱ��ˮ���μ����������İ��̣���֪������Ӧ����N2��ˮ���ɣ����Ԫ�ػ��ϼ۵������غ㣬��֪�Ȼ�狀�п��1��1ǡ�÷�Ӧ������пʣ�࣬��Ӧ�ų���������ѧ����ʽӦΪ��B��NH4NO3+Zn=N2+2H2O+ZnO����������������п���ǽ���п���ٴӷ�Ӧ���̷�����ˮ���˴���������ʹ��ӦѸ�ٷų��������ȣ�����������ܽ����ȣ��ʢٴ��ڸ��ݷ����ķ�ӦNH4NO3+Zn=N2+2H2O+ZnO�����ϼ����ߵ��У�Zn��Zn2����2e����NH4����N2��3e�������ϼ۽��͵�Ϊ��NO3����N2��5e�������Ը��ݵ����غ��֪��ÿ��ԭ1mol NO3��������1molNH4����1mol Zn���ʢ���ȷ���۳�������������п������п������������ʢ���ȷ���ܳ�����������������������пС������п����������ԭ��Ӧ�����غ��ж�ȫ����Ӧ�����Գ������ʲ���Сп�����ʢܴ��������������ڢ���ȷ����ѡB��
=1��1��ʹ��ʱ��ˮ���μ����������İ��̣���֪������Ӧ����N2��ˮ���ɣ����Ԫ�ػ��ϼ۵������غ㣬��֪�Ȼ�狀�п��1��1ǡ�÷�Ӧ������пʣ�࣬��Ӧ�ų���������ѧ����ʽӦΪ��B��NH4NO3+Zn=N2+2H2O+ZnO����������������п���ǽ���п���ٴӷ�Ӧ���̷�����ˮ���˴���������ʹ��ӦѸ�ٷų��������ȣ�����������ܽ����ȣ��ʢٴ��ڸ��ݷ����ķ�ӦNH4NO3+Zn=N2+2H2O+ZnO�����ϼ����ߵ��У�Zn��Zn2����2e����NH4����N2��3e�������ϼ۽��͵�Ϊ��NO3����N2��5e�������Ը��ݵ����غ��֪��ÿ��ԭ1mol NO3��������1molNH4����1mol Zn���ʢ���ȷ���۳�������������п������п������������ʢ���ȷ���ܳ�����������������������пС������п����������ԭ��Ӧ�����غ��ж�ȫ����Ӧ�����Գ������ʲ���Сп�����ʢܴ��������������ڢ���ȷ����ѡB��
�����Ѷȣ�һ��
3�������� ��16�֣�ij1L��Һ�к��д�����Cl����Br����I��������1L����Һ��ͨ��һ��������������Һ��Cl����Br����I�������ʵ�����ͨ������������(��״��)������ϵ���±���ʾ����������д���пհף�
V��Cl2��(�����L)
| 2.8
| 5.6
| 11.2
|
n(Cl��) /mol
| 1.5
| 1.75
| 2.25
|
n(Br��) /mol
| 1.5
| 1.4
| 0.9
|
n(I��)/mol
| a
| 0
| 0
|
�ŵ�ͨ�����������Ϊ2.8Lʱ����Һ�з��������ӷ�Ӧʽֻ�У�?
�Ʊ���a��ֵΪ?
��ԭ��Һ��Cl����Br����I�����ʵ���֮��Ϊ?
��ԭ��Һ��I�������ʵ���Ũ��Ϊ?
�ο��𰸣���16�֣�
��Cl2+2I�D��2Cl�D+I2��0.15��1.25��1.5��0.4��25��30��8������𰸾������֣���0.4mol/L
�����������ȷ������I���Ļ�ԭ��ǿ��Br��������ֻ�е�I���Ƚ���������Ӧ��Ȼ�����Br����������Cl2+2I�D��2Cl�D+I2? Cl2+2Br�D��2Cl�D+Br2
��1����ͨ�����������Ϊ2.8Lʱ����Һ�л�ʣ��I��������ֻ��I����������
��2�����ڶ���ͨ������2.8L��0.125mol��ʱ��I������ȫ��������Br��Ҳ��������0.1 mol
Cl2?+? 2Br�D?��2Cl�D+Br2
0.05mol? 0.1mol
����I����Ӧ������Ϊ0.125mol-0.05mol=0.075mol
Cl2?+? 2I�D��2Cl�D+I2
0.075mol? 0.15mol
���Ա���a��ֵΪ0.15mol
��3����һ��ͨ������2.8Lʱ��I������ʣ�࣬��ֻ�����ˣ�
Cl2?+? 2I�D?��? 2Cl�D?+? I2
0.125mol? 0.25mol? 0.25mol
��ԭ��Һ�У�
����I�� 0.25mol + 0.15mol=0.4mol����Br����1.5mol��Cl�D��1.5mol��0.25mol=1.25mol
��ԭ��Һ��I�������ʵ���Ũ��Ϊ0.4mol/1L=0.4mol/L
�����Ѷȣ�һ��
4������� I.��֪������������ԭ��Ӧ��Zn+2HNO3+NH4NO3��N2��+Zn(NO3)2+3H2O����
��1���÷�Ӧ�Ļ�ԭ��Ϊ������������������ԭ����Ϊ������������������д��ѧʽ��
��2����������N2�ڱ�״�������Ϊ2.24L����Ӧ��ת�Ƶĵ�����Ϊ��������NA��
II.��6�֣���ѧ�����ǵ�����������أ����û�ѧ����ʽ�������������е�ʵ����
��1��ʢ��NaHCO3�ĸɷ�������������?
��2�����ʲ˵��ġ���𡱹��գ������ȵIJ˵�����ˮ�м�����ȴ?
��3�����������õ�����ˮ���뾭��̫����ɹ�����ʹ��??
�ο��𰸣�I.(6��)��1��Zn��NH4NO3�����֣�������N2�����֣����� ����2��0.5��2�֣�
II.��6�֣� ��1��2NaHCO3 ?Na2CO3��CO2����H2O?
?Na2CO3��CO2����H2O?
(2)3Fe��4H2O  Fe3O4��4H2? (3)2HClO
Fe3O4��4H2? (3)2HClO 2HCl��O2��?��ÿ��2�֣�
2HCl��O2��?��ÿ��2�֣�
���������I. ��1��Zn��NH4NO3��NH4+�е�NԪ�أ����ϼ����ߣ��Ƿ�Ӧ�Ļ�ԭ����N2���������������ǻ�ԭ���
��2��2.24L��0.1mol����Ӧ��ת�Ƶĵ�����Ϊ0.5NA��
II. ��1������NaHCO3�����ֽ�������CO2��ԭ��������ʽΪ2NaHCO3 ?Na2CO3��CO2����H2O��
?Na2CO3��CO2����H2O��
��2������Fe�ڸ�����������ˮ������Ӧ��ԭ��������ʽΪ3Fe��4H2O  Fe3O4��4H2��
Fe3O4��4H2��
��3����������������ˮ�к���HClO����HClO����ǿ�����Ե������ֽ⣬��ɹ�����ʹ�ã�����ʽΪ2HClO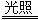 2HCl��O2����
2HCl��O2����
���������⿼��������ԭ��Ӧ��Ӧ�úͻ�ѧ����������֪ʶ��Ҫ��ѧ�����з����ͽ��������������Ѷ��еȡ�
�����Ѷȣ�һ��
5������� ��16�֣�д�����з�Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ��
��1��Ư����Һ��ͨ������Ķ�����̼�Ļ�ѧ����ʽ ___________________________
��2������������ͨ�뵽�廯������Һ�е����ӷ���ʽ_________________________________
��3�����Ṥҵ�������ڽӴ����з����ķ�Ӧ�Ļ�ѧ����ʽ_____________________________
��4��̼��Ũ���ᷴӦ�Ļ�ѧ����ʽ__________________________________
�ο��𰸣�
��1�� Ca(ClO)2 + 2CO2 + 2H2O = 2HClO? +? Ca(HCO3)2
��2��3Cl2 + 2Fe2+? +? 4Br-? =? 6Cl- + 2Fe3+? +? 2Br2
��3��4FeS2 +11O2 ?2Fe2O3 + 8SO2
?2Fe2O3 + 8SO2
��4��SO2 + Br2 + 2H2O? =? 2HBr? + H2SO4
���������
��1��������̼������ǿ�ڴ����ᣬ��Ca(ClO)2 + CO2 + H2O =" 2HClO" + CaCO3�������ǹ����Ķ�����̼��CO2 + H2O + CaCO3 = Ca(HCO3)2����ʽ����ȥ��̼��Ƽ��ɡ�
��2�������������������������ӣ���д������ʽ��3Cl2+2FeBr2=2FeCl3+2Br2��Ȼ��ij����ӷ���ʽ��
��3���������õ��ǻ�����FeS2�ȶ��պ����ɶ��������ٽ�һ��������������������Ũ�����������ɵ����������ڽӴ�������4FeS2+11O2=�����£�2Fe2O3+8SO2����ƽʱҪע����������Ԫ�ر�ۡ�
��4������±��Ԫ�أ��������뵽����ǿ�����ԣ�����ԭ��Br-������������ԭ��Ӧ���ص㣬���������ֻ�ԭ�ԣ�����Һ��������SO42-����ʽ���ڣ���д��Br2+SO2��2Br-+ SO42-��ʣ��IJ���ͨ��ԭ���غ㲹�㡣
�����Ѷȣ�һ��