1、填空题 1 mol单质A与足量盐酸反应,生成22.4L气体(标准状况下),并且元素A转化成与氖的电子层结构相同的离子,据以上事实,回答问题。
(1)元素A的原子结构示意图?。
(2)元素A的最高价氧化物的水化物与盐酸反应的离子方程式?。
(3)举出二个实验事实比较Na与元素A的金属性强弱?、
?。
参考答案:
(1)?(2)Mg(OH)2+H2=Mg2++H2O
(3)Na、Mg分别与H2O反应(其它答案合理也可,下同
本题解析:略
本题难度:简单
2、选择题 某元素R的阴离子R2-核外共有a个电子,核内有b个中子,则表示R原子组成符号正确的是?
A.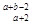 R
R
B.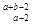 R
R
C. R
R
D.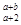 R
R
参考答案:B
本题解析:元素R的质子数为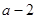 ,其质量数为
,其质量数为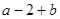 ,所表示R原子组成符号正确的是
,所表示R原子组成符号正确的是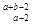
本题难度:一般
3、选择题 下列几组最高价氧化物的水化物,酸性由强到弱顺序排列的是 ?(? )
A.H3PO4 HBrO4 H2SO4 H2CO3
B.H2SiO3 H2CO3 H2GeO3 H3AlO3
C.H2SO4 H2TeO4 HClO4 H2SeO4
D.HClO4 H2SeO4 H2AsO4 H2SbO4
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列各组中互为同位素的是(?)。
A.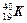 与
与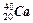
B.T2O与H2O
C.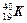 与
与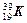
D.金刚石与石墨
参考答案:C
本题解析:略
本题难度:简单
5、推断题 (10分)A、B、C、D、E都是短周期元素,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是?乙物质的电子式是__________
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是_________ (用元素符号填写)
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是?
(4)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,其中有一种产物是TiC(在火箭和导弹上有重要应用)其反应方程式为?
参考答案:(1)第三周期第IIA族?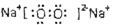 ?
?
(2)O<N<Al<Mg<Na
(3)2 Al + 2OH― + 2H2O = 2AlO2― + 3H2↑
(4)4Al + 3C +3TiO2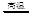 2Al2O3 +3TiC
2Al2O3 +3TiC
本题解析:根据“E是地壳中含量最高的金属元素”确定E为Al;根据“A原子的最外层电子数比次外层电子层多3个”确定A为N;根据“C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。”确定B为O,C为Na,最后根据“A、B、C、D、E都是短周期元素,原子序数逐渐增大”确定D为Mg;据此便可回答相关问题。
本题难度:一般